微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 如果你家里的食用花生油混入了大量的水,利用你所学的知识,采用最简便的分离方法是

A???????????????????????B?????????????????????C??????????????????????????D
参考答案:B
本题解析:略
本题难度:一般
2、选择题 白酒,食醋,蔗糖,淀粉等均为家庭厨房中常用的物质,利用这些物质能完成下列实验的是
A.鉴别食盐和小苏打
B.检验自来水中是否含氯离子
C.检验雨水的酸碱度
D.白酒中是否含甲醇
参考答案:A
本题解析:
试题分析:小苏打是碳酸氢钠,而食醋中含有乙酸,能和碳酸氢钠反应生成CO2气体,而食盐是氯化钠,和食醋是不反应的,A可以鉴别;检验氯离子,需要硝酸酸化的硝酸银溶液,B不能鉴别;检验雨水的酸碱度需要pH试纸,C不能鉴别;白酒、食醋、蔗糖和淀粉都不能鉴别白酒中的甲醇,D不正确,因此正确的答案选A。
点评:物质的检验一般依据物质的性质,特别是化学性质。即进行物质的检验时,要依据物质的特殊性质和特征反应,选择适当的试剂和方法,准确观察反应中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理、验证即可。
本题难度:一般
3、填空题 某化学实验室产生的废液中含有Fe3+、Cu2+、Ba2+、Cl-四种离子,现设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯化铁晶体。
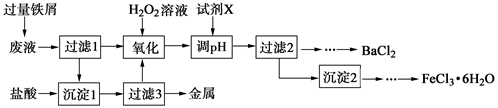
(1)沉淀1中含有的金属单质是???。
(2)氧化时加入H2O2溶液发生反应的离子方程式为???。
(3)下列物质中,可以作为试剂X的是???(填字母)。
A.BaCl2
B.BaCO3
C.NaOH
D.Ba(OH)2
(4)检验沉淀2洗涤是否完全的方法是???。
(5)制备氯化铁晶体过程中需保持盐酸过量,其目的是???。
(6)由过滤2得到的滤液制备BaCl2的实验操作依次为???、冷却结晶、???、洗涤、干燥。
参考答案:(1)铁、铜(2分,各1分)
(2)2Fe2++2H+
本题解析:
试题分析:(1)加入铁屑能把铜置换出来,同时又铁剩余,沉淀为铁、铜;(2)流程中需把亚铁离子氧化为铁离子后再沉淀除去,双氧水氧化Fe2+;(3)加入X试剂是为了调节pH使铁离子生成氢氧化铁沉淀,为了不引入新杂质可以加入BaCO3、Ba(OH)2等物质;(4)检验沉淀洗涤是否干净一般应取最后次的滤液检验可能含有的杂质离子,一般检验硫酸根离子、氯离子等;(5)氯化铁在水溶液中水解,加如盐酸过量能抑制Fe3+水解;(6)过滤后得到的溶液为稀溶液,从溶液中得到晶体可以采用蒸发浓缩降温结晶的方法。
本题难度:一般
4、选择题 向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是
?
| 操作
| 现象
| 结论
|
A
| 滴加氯水和CCl4,振荡、静置
| 下层溶液显紫色
| 原溶液中有I-
|
B
| 向溶液X 中先滴加稀硝酸,再滴加Ba(NO3)2溶液
| 出现白色沉淀
| 溶液X 中一定含有SO42-
|
C
| 用洁净铂丝蘸取溶液进行焰色反应
| 火焰呈黄色
| 原溶液中有Na+、无K+
|
D
| 滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口
| 试纸不变蓝
| 原溶液中无NH4+
?
参考答案:A
本题解析:
试题分析:A、I2易溶于CCl4且溶液显紫色;B、若溶液中含有SO32-也可以被HNO3氧化为SO42-而产生白色沉淀;C、未通过蓝色钴玻璃不能判断K+是否存在;D、NH3易溶于水,选用稀NaOH溶液不利于NH3的放出。
本题难度:一般
5、选择题 已知 、 、 、 、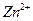 较完全地形成氢氧化物沉淀,溶液的pH分别为3.7、9.6、4.4左右。某硫酸锌酸性溶液中含有少量 较完全地形成氢氧化物沉淀,溶液的pH分别为3.7、9.6、4.4左右。某硫酸锌酸性溶液中含有少量 、 、 杂质离子,为除去这些离子制得纯净的硫酸锌,应加入的试剂是: 杂质离子,为除去这些离子制得纯净的硫酸锌,应加入的试剂是:
A. 溶液 溶液
B. 、 、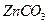
C.氨水
D. 、 、
参考答案:D
本题解析:略
本题难度:简单
|