微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (22分)草木灰中富含钾盐,主要成分是碳酸钾,还含有少量氯化钾、硫酸钾。现从草木灰中提取钾盐,并用实验检验其中的 CO32―、 SO42―和 Cl―。
(1)从草木灰中提取钾盐的实验操作顺序如下:①称取样品,②溶解,③??????????,④?????????????,⑤冷却结晶。
(2)将制得的少量晶体放入试管,加入蒸馏水溶解并把溶液分成三份,分装在3支试管里。
①在第一支试管里加入稀盐酸,可观察有???????生成,证明溶液中有????????离子。
②在第二支试管里加入足量稀盐酸后,再加入??????????,可观察到有????????生成,证明溶液中有????????离子;写出相关的化学方程式??????????????????????????;
判断所加入稀盐酸已经足量的方法是_____________??_________???????????????_。
③在第三支试管里加适量的硝酸银,观察到有沉淀产生,由此证明溶液中一定含Cl―、。你认为该结论是否严密?为什么?
???????????????????????????????????????????????????????????????。
参考答案:(22分)(1)②过滤,取滤液;(2分) ③蒸发滤液(2分)
本题解析:(1)草木灰中含有不溶性杂质,所以溶解后应该是过滤;然后将滤液蒸发结晶即可。
(2)①碳酸盐能和盐酸反应生成CO2,所以如果出现气泡,则说明含有CO32-;
②检验SO42-的方法是先加入盐酸,然后再加入氯化钡溶液,观察产生的白色沉淀即可;先加入盐酸,首先和溶液中的碳酸钾反应,方程式是2HCl+K2CO3=2KCl+H2O+CO2↑;而氯化钡与硫酸钾反应的方程式是K2SO4+BaCl2=2KCl+BaSO4↓;判断盐酸是否过滤的方法是继续加入盐酸,即继续滴入稀盐酸,溶液中不再产生气体,就说明盐酸已知过量。
(3)由于碳酸根离子、硫酸根离子也会与银离子作用产生白色沉淀,所以不能通过白色沉淀来说明含有氯离子。
本题难度:一般
2、选择题 下列各物质(括号内物质为杂质)?的除杂质方案设计中,合理的是( )
A.NO2(NO):通入足量O2充分反应
B.CO2(SO2):通过饱和Na2CO3溶液?
C.Na2SO3溶液(Na2SO4):滴加适量的BaCl2溶液
D.Na2CO3固体(NaHCO3):充分加热
参考答案:A.由于不能确定NO的物质的量,易混入氧气,故A错误;
本题解析:
本题难度:一般
3、实验题 钛(Ti)具有高强度和耐酸腐蚀性,是重要的工业原料。以金红石(主要成分为TiO2,含少量Fe2O3、SiO2)为原料可制取Ti。工业流程如下:
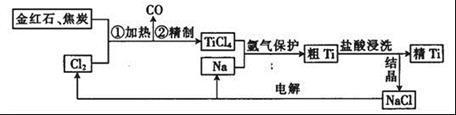
(1)粗TiCl4中含有少量FeCl3、SiCl4等,它们的部分性质如下:

从粗TiCl4中精制TiCl4的方法是________(填字母)。
A.用水溶解后,重结晶??? B.蒸馏??? C.用乙醚萃取后,分液
(2)写出用惰性电极电解熔融NaCl时阳极的电极反应式:_________________;阴极产物是__________。
(3)Ti可溶解在浓HF溶液中,请完成下列离子方程式:

(4)如图是一个制取氯气并以氯气为原料进行反应的装置,
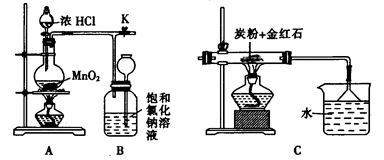
①装置A中发生反应的化学方程式为_____________________________________。
②在实验室中,某同学欲用如图所示装置净化氯气,则M、N中应盛放的试剂分别是__________、__________。(填试剂名称)

③实验开始时,先点燃A处的酒精灯,打开旋塞K,让C12充满整个装置,再点燃C处酒精灯。Cl2通过装置M、N再进入装置C,与装置C中的固体粉末发生氧化还原反应生成CO气体。试写出装置C中发生反应的化学方程式:_________________________。
参考答案:(14分)
(1)B(3分)
(2)2Cl- -
本题解析:
试题分析:
(1)结合杂质的性质,可以看出熔沸点相差较大,可采用蒸馏的方法;
(2)惰性电极电解熔融NaCl时阳极放电的Cl-,2Cl- -2e-= Cl2↑;阴极产物为钠。
(3)根据化合价变化情况可得:分别为1,6.1.2H+,2
(4)①实验室制取氯气的反应4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
②除去氯气中氯化氢用饱和食盐水,干燥可用浓硫酸。
③根据题意可得反应为:TiO2+2C+2 Cl2 ?TiCl4 +2CO
?TiCl4 +2CO
本题难度:一般
4、选择题 下列每项中各有3组物质,它们都能用分液漏斗分离的是[???? ]
A.乙酸乙酯和水、酒精和水、苯酚和水
B.二溴乙烷和水、溴苯和水、硝基苯和水
C.甘油和水、乙酸和乙醇、乙醛和水
D.油酸和水、甲苯和水、乙烷和水
参考答案:B
本题解析:
本题难度:简单
5、选择题 为提纯下列物质(括号中为杂质),所选除杂试剂和分离方法都正确的是( )
| 选项 | 被提纯的物质(杂质) | 除杂试剂 | 分离方法
A
NH3(H2O)
浓硫酸
洗气
B
H2O(Br2)
CCl4
分液
C
KCl固体(I2)
KOH溶液
加热
D
苯(苯酚)
浓溴水
过滤
A.A
B.B
C.C
D.D
参考答案:D
本题解析:
本题难度:一般
|