��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����й�Na2CO3 ��NaHCO3�����ʱȽ��У��������
A�����ȶ��ԣ�Na2CO3 >NaHCO3
B���ܽ�ȣ�Na2CO3<NaHCO3
C�������ᷴӦ�����ʣ�Na2CO3 <NaHCO3
D����Է�������Na2CO3 >NaHCO3
2��ѡ���� ��֪�Ȼ�ѧ����ʽ��H+��aq��+OH-��aq��= H2O(l)???��H 1= -57.3 kJ/mol
1/2H2SO4��Ũ��+ NaOH��aq��=" 1/2" Na2SO4��aq��+ H2O(l)?��H 2 = m������˵����ȷ����???��????��
A�������Ȼ�ѧ����ʽ�еļ�������ʾ������
B����H 1>��H 2
C����H 2= -57.3 kJ/mol
D���O��H 1 �O>�O��H 2�O
3��ѡ���� �����й�����ת������ʶ����ȷ����
A��ֲ��Ĺ������ʹ̫����ת��Ϊ��ѧ��
B������ʹ�������豸��Ҫ�ǽ�����ת��Ϊ����
C��ȼ��ȼ��ʱֻ�ǽ���ѧ��ת��Ϊ����
D���������ڵĻ�ѧ�仯�����������ϱ������ⷢ����һЩ����ת������������Ч
4������� (6��)�ڻ���ƽ�����װ�л�ԭ���£�N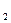 H
H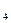 ����ǿ������H
����ǿ������H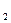 O
O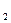 �������ǻ��ʱ�������������ĵ�����ˮ���������ų��������ȡ���֪0.4 mol Һ̬�º�����Һ̬H
�������ǻ��ʱ�������������ĵ�����ˮ���������ų��������ȡ���֪0.4 mol Һ̬�º�����Һ̬H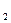 O
O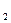 ��Ӧ���ɵ�����ˮ����ʱ�ų�256.64 kJ��������
��Ӧ���ɵ�����ˮ����ʱ�ų�256.64 kJ��������
(1)д��Һ̬�º�Һ̬H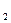 O
O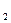 ��Ӧ���Ȼ�ѧ����ʽ?????????????????????????????????��
��Ӧ���Ȼ�ѧ����ʽ?????????????????????????????????��
(2)��֪H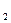 O��l��="===" H
O��l��="===" H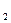 O(g)����H=+44kJ/mol����16 gҺ̬��������Һ̬H
O(g)����H=+44kJ/mol����16 gҺ̬��������Һ̬H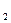 O
O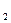 ��Ӧ���ɵ�����Һ̬ˮʱ���ų���������_____________________��
��Ӧ���ɵ�����Һ̬ˮʱ���ų���������_____________________��
(3)������ӦӦ���ڻ���ƽ��������ͷų����������Ϳ��ٲ������������⣬����һ����ͻ�����ŵ���_______________________________________________________________��
5������� ��10�֣���ͼ�ǹ�ҵ��������淋����̡�
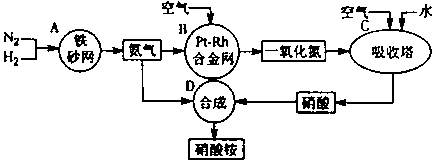
��1��������C��ͨ�������Ŀ����??????????????????????????????????��
A��B��C��D�ĸ������еķ�Ӧ������������ԭ��Ӧ����???????������ĸ����
��2����֪��4NH3��g��+3O2��g��=2N2��g��+6H2O��g��??��H = ��1266��8kJ��mol
N2��g��+O2��g��=2NO��g��?????????��H="?" +180��5 kJ��mol
д�������´��������Ȼ�ѧ����ʽ��???????������������Ӧ�Ļ�ѧƽ�ⳣ������ʽK=?????��
��3����֪��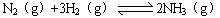 ???��H= ��92 kJ��mol��Ϊ���������ת���ʣ��˲�ȡ�Ĵ�ʩ��???????��������ĸ��
???��H= ��92 kJ��mol��Ϊ���������ת���ʣ��˲�ȡ�Ĵ�ʩ��???????��������ĸ��
A�������¶�???????? B��ʹ�ô���??????? C������ѹǿ
D��ѭ�����úͲ��ϲ��䵪��??? E����ʱ�Ƴ���
��4����һ���¶Ⱥ�ѹǿ�£���H2��N2��3��1������ȣ����ܱ������л�ϣ����÷�Ӧ�ﵽƽ��ʱ�����ƽ��������NH3�������������Ϊ17��6������ʱH2��ת����Ϊ????????��