微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 实验室以空气(O2体积分数20%)为原料,在无碳、无水的环境下,用下图A装置制备臭氧(3O2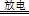 2O3)。
2O3)。
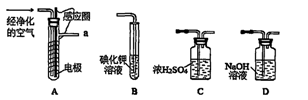
(1)空气通入A装置之前,应先后通过上述装置中的???????、???????(填装置序号)。
(2)臭氧与碘化钾溶液反应为:2KI+O3+H2O=2KOH+I2+O2。将a处气体通入装置B,溶液中的现象为???????????????。
(3)为测定O2转化为O3的转化率,将装置B中的溶液全部转入另一容器中,加入CC14,经萃取、分液、蒸馏、冷却、称重,得I2固体0.254g。
①萃取操作所用玻璃仪器的名称???????。
②若实验时通入空气1.12L(标准状况),O2的转化率为???????。
③测定时需在A、B装置间连接装置D,原因是???????。
(4)工业上分离O3和O2,可将混合气体液化后再分离,下列分离方法合理的是???????(填序号)。
A.过滤 B.分馏 C.分液 D.萃取
(5)臭氧可用于含CN一碱性电镀废水的处理。第i步:CN一转化为OCN-;第ii步:OCN一继续转化为CO32一及两种单质气体。若第ii步转化时,O3与OCN-物质的质量之比为3∶2,该步反应的离子方程式为???????。
参考答案:(15分)(1)D、C(各1分,2分)??
(2)溶液
本题解析:
试题分析:(1)根据无碳无水环境条件,则空气通入A装置前应先后通过NaOH溶液、浓H2SO4的洗气瓶;(2)a处气体通入B,臭氧能氧化KI,溶液中因生成的I2变黄;(3)①萃取使用分液漏斗、烧杯;②由m/M可知n(I2)=0.254g÷254g/mol=0.001mol,由2KI+O3+H2O=2KOH+I2+O2可知,n(O3)=0.001mol,由3O2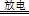 2O3可知,n(O2)=0.0015mol,由V/Vm可知n(空气)=0.05mol,由空气的组成可知,n(O2)=0.01mol,因此O2得转化率为0.0015÷0.01×100%=15%;③NaOH溶液能除去空气中氮气和氧气在放电时产生的氮氧化物,防止NO2与KI溶液反应;(4)臭氧和氧气先液化,二者沸点不同,可用分馏的方法分离,故B正确;(5)第一步反应中碳元素由+2价升为+4价,第二步反应中氮元素由―3价升为0价,部分氧元素由0价将为―2价,则两步反应分别为O3+CN―=OCN―+O2、2OCN―+2OH―+3O3=2CO32一+N2+3O2+H2O。
2O3可知,n(O2)=0.0015mol,由V/Vm可知n(空气)=0.05mol,由空气的组成可知,n(O2)=0.01mol,因此O2得转化率为0.0015÷0.01×100%=15%;③NaOH溶液能除去空气中氮气和氧气在放电时产生的氮氧化物,防止NO2与KI溶液反应;(4)臭氧和氧气先液化,二者沸点不同,可用分馏的方法分离,故B正确;(5)第一步反应中碳元素由+2价升为+4价,第二步反应中氮元素由―3价升为0价,部分氧元素由0价将为―2价,则两步反应分别为O3+CN―=OCN―+O2、2OCN―+2OH―+3O3=2CO32一+N2+3O2+H2O。
本题难度:一般
2、填空题 取少量Fe2O3粉末(红褐色)加入适量盐酸,化学反应方程式为:?????????????????????????????????????,得到棕黄色的FeCl3溶液,用此溶液分别做如下实验:在小烧杯中加入20 mL蒸馏水,煮沸后,滴入几滴FeCl3溶液,继续煮沸至溶液呈红褐色,即制得??????????????????????,用激光笔照射烧杯中的液体,可以观察到液体中出现?????????????????,这个现象叫????????????????????????。
参考答案:.(共5分)Fe2O3 + 6H+ =2Fe3++3H2O;
本题解析:
试题分析:氧化铁是碱性氧化物,能和盐酸反应,方程式是Fe2O3 + 6H+ =2Fe3++3H2O;在小烧杯中加入20 mL蒸馏水,煮沸后,滴入几滴FeCl3溶液,继续煮沸至溶液呈红褐色,即制得氢氧化铁胶体,用激光笔照射烧杯中的液体,可以观察到液体中出现光亮的通路,这个现象叫丁达尔效应。
点评:该题是基础性试题的考查,试题难易适中,侧重对学生基础知识的巩固和训练。有助于培养学生的应试能力,提高学生分析问题、灵活运用基础知识解决实际问题的能力。该题难度不大,学生记住即可得出正确的结论。
本题难度:一般
3、选择题 下列说法正确的是( )
①氯气有漂白性 ②实验室制取氯气时,为了防止环境污染,多余的氯气可以用氢氧化钙溶液吸收 ③新制氯水的氧化性强于久置氯水 ④除去HCl气体中的Cl2,可将气体通入饱和食盐水⑤氯气的水溶液呈酸性
A.①②③
B.②③
C.③④
D.③⑤
参考答案:D
本题解析:
试题分析:①干燥的氯气没有漂白性,错误。
②实验室制取氯气时,为了防止环境污染,多余的氯气可以用氢氧化钠溶液吸收,氢氧化钙溶液浓度太低。错误。
③新制氯水含有氯气、次氯酸,久置氯水其实是盐酸溶液,所以新制氯水的氧化性强于久置氯水。正确
④除去HCl气体中的Cl2,将气体通入饱和食盐水不行,因为HCl易溶于水。错误。
⑤氯气的水溶液含有HCl、HClO呈酸性,正确。
点评:掌握氯气的性质,新制氯水与久置氯水的区别。
本题难度:一般
4、实验题 醛可与NaHSO3饱和溶液发生加成反应,生成水溶性的α-羟基磺酸钠:
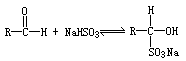
反应是可逆的。在通常条件下有70%~90%的原料向正反应方向转化。
(1)若氯苯中含有杂质苯甲醛,要除去此杂质,可作用的试剂是____,反应的化学方程式为:____;分离的方法是____。
(2)若使CH3―CHOH―SO3Na转化为乙醛,可采用的试剂是____,反应的化学方程式为____,分离的方法是____。
参考答案:
 本题解析:充分应用题给信息,并联想有关化学平衡移动的概念和物质的性质分析题目要求。
本题解析:充分应用题给信息,并联想有关化学平衡移动的概念和物质的性质分析题目要求。
(1)氯苯中混有苯甲醛,按题给反应,用NaHSO3与苯甲醛加成,生成可溶于水的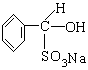 ,则与不溶于水的氯苯分为两层,用分液漏斗分离即可。反应的化学方程式为:
,则与不溶于水的氯苯分为两层,用分液漏斗分离即可。反应的化学方程式为:
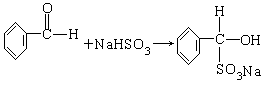
(2)注意到题给条件“反应是可逆的,在通常条件下”正反应方向的转化率较高,若能使平衡左移,则可生成乙醛,而考虑平衡左移的方法,若以CH3―CHOH―SO3Na为纯液体,没有浓度的问题,则只应考虑使左侧NaHSO3浓度减小的办法,则可相应使用H2SO4,发生反应:
2NaHSO3+H2SO4==Na2SO4+2H2O+2SO2↑
使NaHSO3浓度减小,而使平衡左移,转化为乙醛:

注意到Na2SO4为离子晶体,熔沸点较高,而CH3CHO沸点仅为20.8℃,易挥发,所以用蒸馏的方法,则可分离出乙醛。
本题难度:一般
5、实验题 某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
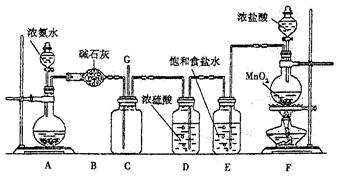
请回答下列问题:
(1)装置A中的烧瓶内固体不可以选用???????????????(选填序号)。
A.生石灰????????? B.碱石灰???????? C.五氧化二磷????????? D.烧碱
(2)B装置的作用??????????????????????????;E装置的作用????????????????????。
(3)通入C装置的两根导管左边较长、右边较短,目的是???????????????????????????。
(4)装置F中发生反应的化学方程式是????????????????????????????????????????。
(5)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出反应的化学方程式:?????????????????????????????????????????????????????。
(6)从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,如何处理?
??????????????????????????????????????????????????????????????????????????????????????。
参考答案:(1)C;(2)干燥氨气;除去氯气中的氯化氢;(3)使密度较
本题解析:(1)装置A制取氨气,可用浓氨水与碱石灰(或烧碱或生石灰等),但部能用五氧化二磷,因其与水反应后生成磷酸,能与氨水反应;(2)B装置中盛放的碱石灰,用来干燥氨气;E装置中盛放的饱和食盐水,用来除去氯气中混有的氯化氢气体;(3)由于氨气的密度小,氯气的密度大,密度小氨气的从长管进入向上扩散,密度大的氯气从短管进入向下扩散,这样能较快的充分的混合;(6)黄绿色的气体是氯气,依据氯气的性质,可用烧碱溶液吸收。
本题难度:简单