��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ͼ��һ��ʵ��������װ�ã������ڷ�����������ռ��������� (?? )
����֪�м�Ĺ��ƿ��װ����Ũ���ᣩ
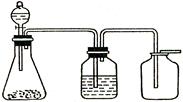
A������ʯ��ϡ����
B���������̺�Ũ����
C������ϡ����
D���������ƺ�ˮ
�ο��𰸣�D
���������
���������̼��ƺ�ϡ���ᷴӦ��������ƣ���������������ʣ�������̼��Ʊ��棬�Ƿ�Ӧֹͣ�����������Ʊ�CO2���壻�������̺�Ũ�����Ʊ�������Ҫ���ȣ��������ᷴӦ�������������������ܶ�С�ڿ����ģ�Ӧ���������ſ������ռ����������ƺ�ˮ��Ӧ��������������Ũ������Ҳ�����������ſ������ռ���������ȷ�Ĵ�ѡD��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣�����ۺ���ǿ�����ض�ѧ������֪ʶ�Ĺ��̺�ѵ�����������������Ϲ淶�Ͻ���ʵ���������������Ĺؼ���������ס����������Ʊ�ԭ����װ�á��ռ������Լ���������ȣ�Ȼ��������������ü��ɡ�
�����Ѷȣ���
2��ʵ���� �����������ػ�ɫ�̼������壬�۵㣺��116�棬�е�3.8�森�������Ȳ��ȶ����Ӵ�һ���л����ױ�ը����������ˮ��1��100����ͬʱ��Ӧ���ɴ�������Һ���Ʊ���֮��Ҫ��ȴ�ɹ�̬�Ա���������森�Ʊ�����Cl2O�����ø����������HgO��Ӧ��������HgO?HgCl2����װ��ʾ����ͼ������̨�ͼг���������ȥ����
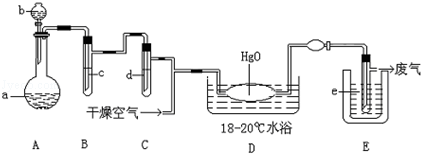
��1��A��ʢ�е���ɫ�����Լ�a����??������Һ©�����Լ�b�� ����????
��2��B��ʢ��Һ��c����???????����C�е�Һ��d����???????????��
��3��D����������Ӧ�Ļ�ѧ����ʽ����???????????????????????????????��
��4��E�еı���ƿ��ʢ�����������Ӧ����??????????�����ڸɱ�����ˮ��Һ̬������ѡ����E���ڹܵõ������������п��ܺ�����������????????????��
��5��װ��A��B��C������ӷ�ʽ��D��E������ӷ�ʽ�����Ե���������������???????????????????????????????????????��������Щ��ͬ�����ӷ�ʽ����Ҫ��������???????????????????????????????????????????????????????����
�ο��𰸣���1��������أ�Ũ���ᣮ��2������ʳ��ˮ��Ũ���ᣮ��3��2H
���������
�����������1����װ��ͼ��֪��A�з�����Ӧ�Ʊ���������Ӧ������ȣ���ɫ�����Լ�a����Һb��Ӧ��ͨ��ӦΪ���������Ũ���ᣬ��aΪ������أ�bΪŨ���ᣮ�ʴ�Ϊ��������أ�Ũ���ᣮ��2��HCl�ӷ���A�����ɵ������к���HCl��H2O���ñ���ʳ��ˮ����HCl����Ũ�������ȳ��Ȼ��⣬������B��ʢ��Һ��c���Լ�����ʳ��ˮ��C�е�Һ��d��Ũ���ᣮ�ʴ�Ϊ������ʳ��ˮ��Ũ���ᣮ��3������Ϣ��֪��D��������HgO��Ӧ����Cl2O��HgO?HgCl2����Ӧ����ʽΪ2HgO+2Cl2=Cl2O+HgO?HgCl2���ʴ�Ϊ��2HgO+2Cl2=Cl2O+HgO?HgCl2����4������Ŀ��Ϣ��֪����������������۵㩁116�棬�۵�ܵͣ�����ѡ��е�ܵ͵�Һ̬�����������䣮���ݹ������̿�֪��D�з�Ӧ�������ܲ��ܳɷַ�Ӧ������������Һ��������E���ڹܵõ������������п��ܺ���������Һ�ȣ��ʴ�Ϊ��Һ̬������Һ�ȣ���5������Ϣ��֪���������Ȳ��ȶ����Ӵ�һ���л����ױ�ը����� Cl2O�������л���Ӵ�������A��B��C�����齺�����ӣ�D��E�䲻���齺�����ӣ��ʴ�Ϊ��A��B��C�����齺�����ӣ�D��E�䲻���齺�����ӣ�Cl2O���л����ױ�ը��
�����Ѷȣ�һ��
3��ѡ���� ����ҩƷ��װ�ú������������Ӧʵ�����??????
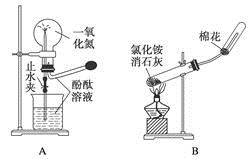
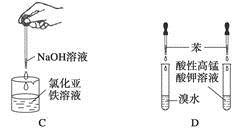
A����Ȫʵ��
B��ʵ������ȡ���ռ�����
C���Ʊ�����������
D����֤�����Ƿ���̼̼˫��
�ο��𰸣�D
���������NO������ˮ��Ҳ����ˮ��Ӧ���ʲ���������Ȫʵ�飬A������ȹ�������ʱ���Թܿ�Ӧ��������б��B�����Fe(OH)2���н�ǿ�Ļ�ԭ�ԣ�Ӧ���ιܲ���Һ�����£�C�����ͨ����ˮ�����Ը��������Һ�Ƿ���ɫ��������֤�������Ƿ���̼̼˫����D����ȷ��
�����Ѷȣ�һ��
4��ѡ���� ����������һ����ɫ������Һ�壬����Ҫ��������Ʒ����̽����������
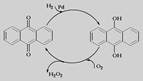
��1�������������ʺ����ϵ�һ����ǩ��?????????????��
?? A?????????????? B?????????????? C??????????????? D
?
 ? ?
��2������������Ʊ������ܶ࣬���з�����ԭ����������ߵ��ǣ�???????????��
A�� BaO 2 + H2SO 4 ="==" BaSO4 �� + H2O2
B�� 2NH4HSO4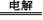 (NH4)2S2O8 + H2���� (NH4)2S2O8 + H2����
Ȼ��ˮ�� (NH4)2S2O8 + 2H2O =2NH4HSO4 + H2O2��
C��CH3CHOHCH3+O2��CH3COCH3+H2O2
D���һ���������
��3����������ȼ�ϵ�ع���ʱ�ɲ����������⣨������ͼ����������̼��Carbon����������С�Բ������������Ũ�ȣ�concentration����Ӱ�죨��Ӱ������������ͼ����
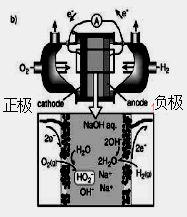 ????? ?????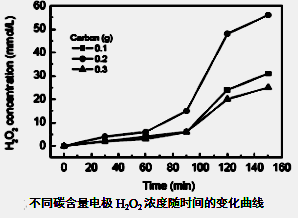
����˵����ȷ����????????????��
A����ʼʱ���ʾ�������˵���缫��һ����Ĺ���
B��һ��ʱ����������ٴ�ƽ����˵��������ֽ�������ƽ��
C������������Һ���ữ��ɷ������������
D��������̼��������0.2g����
��4������������Ϊһ����ɫ�������й㷺Ӧ�ã���д�����з�Ӧ�Ļ�ѧ����ʽ��
���ڹ������������£�ͭ��ϡ����������ͭ��??????????????????????��
����Ti-Si����ɸ���������ױ���������������Ϊ��-�ױ��ӣ�???????? ???��
�ο��𰸣�
��1��B��2��D��3��ABCD ��4����Cu+H2S
���������
���⿼�����������Ʊ�����2��Dѡ������ʿ���ѭ�����ã�ԭ����������ߣ���3�������߿��Կ�����0��90minH2O2�������ߣ�90min������Ͽ죬Aѡ����ȷ��120min���������ʼ�����˵��������ֽ�������ƽ�⣬Bѡ����ȷ��������ӦΪ��H2O��O2��2e��=HO2����OH�������ɵ�HO2�����H�������H2O2��Cѡ����ȷ�����������߱Ƚ�������������̼������0.2gʱ��H2O2�IJ�����ߣ�Dѡ����ȷ����4��H2O2��Ϊǿ��������
�����Ѷȣ�һ��
5��ѡ���� Ϊ�˳�ȥ�����л��е�����ˮ��������ʹ�����ʵ�����ͨ��ij�ض��ĸ���ܣ��˸������װ������ҩƷ�еģ�������
A������������δ
B��Ũ����
C������ʳ��ˮ
D����ʯ��
�ο��𰸣�A������������δ����������Ӧ���ܹ��������������Է��ڸ����
���������
�����Ѷȣ���
|