微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 有某硫酸铜、硫酸亚铁、硫酸铁的混合溶液100 mL,已知溶液中各种阳离子的物质的量相等,硫酸根离子的浓度为7 mol / L。此溶液最多能溶解铁粉的质量为
A.5.6 g
B.10.6 g
C.11.2 g
D.16.8 g
2、填空题 (12分)原子序数由小到大排列的X、Y、Z三种短周期元素,已知三种元素的原子序数之和等于16,单质X2 、Y2 、Z2之间有如下转化关系(反应条件已略)。已知:甲、乙分子中均含有10个电子;丙分子中含有15个电子。请回答:
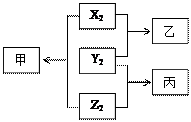
(1)Y2的电子式是___?______;该分子中有??????个σ键,??????个π键。
(2)甲属于(填“极性”或“非极性”)??????分子;晶体中甲分子的配位数为??? ????。
????。
(3)乙分子的VSEPR模型名称为??????????,分子的立体构型名称为????????????。
(4)写出乙与Z2反应生成丙的化学方程式??????????????????????????????。
(5)工业上用氧化铝、碳和乙在1400℃条件下反应,制取由元素Y和Al组成的化合物丁,同时还有CO和X2生成。已知反应中消耗1mol乙,可生成1.5molCO和1.5molX2。写出反应的化学方程式:?????????????????????????????,氧化剂为?????????。
3、选择题 下列叙述不正确的是[???? ]
A.漂白粉的有效成分是Ca(ClO)2
B.胆矾的成分是CuSO4・5H2O
C.医疗上用的“钡餐”成分是BaSO4
D.光导纤维主要成分是Si
4、实验题 某化学实验小组为了验证SO2和Cl2的漂白性,设计了如下图所示的实验装置。请回答下列问题:
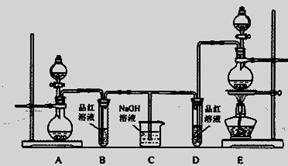
(1)他们制备SO2和Cl2所依据的原理分别是:Na2SO3+H2SO4=Na2SO4+H2O+SO2↑、MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,则上图A、E装置中用来制Cl2的装置是?????
MnCl2+Cl2↑+2H2O,则上图A、E装置中用来制Cl2的装置是?????
(填序号),反应中盐酸所表现的性质是????????;
(2)反应开始后,发现B、D试管中的品红溶液都褪色,停止通气后,给B、D两个试管中的溶液加热,B试管中的现象是??????????;
(3)装置C的作用是?????????;
(4)NaOH(足量)溶液分别与两种气体反应的离子方程式是????????、??????????;
(5)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色。查阅资料得知:两种气体按体积比1∶1混合,再与水反应可生成两种常见酸,因而失去漂白作用。该反应的化学方程式为??????????????。
5、选择题 下列卤素化合物不可能存在的是(???)
A.NaBrO3
B.NaFO
C.HClO4
D.HClO