微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某小组为研究原电池原理,设计如图装置,下列叙述正确的是
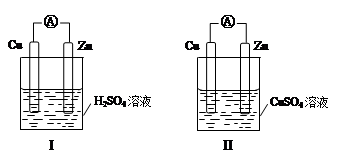
A.装置I,铜片上有O2逸出
B.装置I,锌片溶解,发生还原反应
C.装置II,电池反应为:Zn+ Cu2+= Zn2++ Cu
D.装置II,外电路中,电子从锌电极流向铜电极
参考答案:CD
本题解析:
试题分析:A、装置I为原电池,铜片上有氢气逸出,错误;B、装置I为原电池,锌片溶解作负极,错误;C、装置II中锌作负极,铜作正极,电池反应为锌与铜离子的置换反应,正确;D、原电池装置中,电子从外电路的负极流向正极,正确,答案选CD。
本题难度:一般
2、选择题 将反应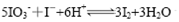 设计成如下图所示的原电池。开始时向甲烧杯中加入少量浓硫酸,电流计指针发生偏转,一段时间后,电流计指针回到零,再向甲烧杯中滴入几滴浓NaOH溶液,电流计指针再次发生偏转。下列判断不正确的是
设计成如下图所示的原电池。开始时向甲烧杯中加入少量浓硫酸,电流计指针发生偏转,一段时间后,电流计指针回到零,再向甲烧杯中滴入几滴浓NaOH溶液,电流计指针再次发生偏转。下列判断不正确的是
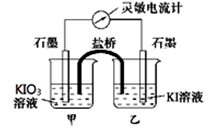
A.开始加入少量浓硫酸时,乙中石墨电极上发生氧化反应
B.开始加入少量浓硫酸时,同时在甲、乙烧杯中都加入淀粉溶液,只有乙烧杯中溶液变蓝
C.电流计读数为零时,反应达到化学平衡状态
D.两次电流计指针偏转方向相反
参考答案:B
本题解析:
试题分析:A、开始向甲中加入少量浓硫酸,反应正向进行,则IO3-会得到电子生成碘单质,所以乙中的石墨电极发生失去电子的氧化反应,正确;B、该反应中的IO3-和I-都转化为碘单质,所以甲、乙烧杯中都加入淀粉溶液后溶液都变蓝色,错误;C、因为该反应为可逆反应,当电流计指针为0时,说明无电流通过,不再发生电子的转移,反应达到平衡状态,正确;D、向甲烧杯中加入NaOH溶液时,则反应逆向进行,碘单质分别生成IO3-和I-,则两极上发生反应的类型不同,电流计的指针的偏转方向相反,正确,答案选B。
考点:考查对电化学反应原理的应用
本题难度:一般
3、选择题 将纯锌片和纯铜片按图示方式插入同浓度同体积的稀硫酸中一段时间,以下叙述正确的是( )
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯的溶液中H+浓度均减小
D.乙装置中化学能转化为电能
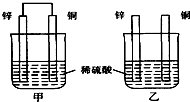
参考答案:A、甲中形成铜锌原电池,锌作负极,失电子,铜作正极,H+在铜
本题解析:
本题难度:一般
4、选择题 将纯锌片和纯铜片按图所示方式插入相同浓度的稀硫酸中,以下有关叙述中正确的是???????????????????????????????????????
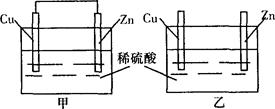
A.甲装置中铜片表面有气泡生成
B.乙装置中电能转化为化学能
C.甲装置中电能转化为化学能
D.乙装置中铜片表面有气泡生成
参考答案:A
本题解析:
试题分析:根据装置图可知,甲装置是原电池,化学能转化为电能。其中锌比铜活泼,做负极失去电子。铜是正极,溶液中的氢离子在正极得到电子生成氢气。乙装置是锌与稀硫酸直接发生的置换反应,但铜和稀硫酸不反应,所以选项A正确,其余选项均是错误的,答案选A。
点评:该题是高考种的常见题型和重要的考点,主要是考查学生对原电池原理、电极名称、电极反应式的了解掌握情况,旨在培养学生灵活运用基础知识解决实际问题的能力。该题的关键是明确原电池的工作原理,然后结合题意和装置图灵活运用即可。
本题难度:简单
5、选择题 如图所示装置中,当闭合K时,下表中装置的描述正确的一项是
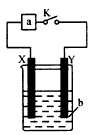 [???? ]
[???? ]
a?
X极材料
Y极材料
? b
对装置的描述
A.
电流表?
石墨
铜
氯化铁溶液
铜为负极,石墨电极质量增加
B.
电流表?
铁
铜
盐酸
电子流动路径是:铁→外电路→铜→
盐酸→铁,从而构成闭合回路
C.
直流电源?
石墨
石墨
硫酸
?溶液的pH始终保持不变
D.
直流电源
?铜
铁
硫酸铜溶液
溶液中Cu2+的浓度可能保 持不变
参考答案:D
本题解析:
本题难度:一般