微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 已知过氧化钠 投入水中能发生下列反应:2Na2O2+2H2O==4NaOH+O2↑。现将7.8g过氧化钠投入水中,充分反应后。计算:
(1)求生成的氢氧化钠的物质的量和氧气的体积。
(2)如反应后得到的溶液中Na+和水分子的个数比为1︰100,则开始时所用的水的质量是多少g?
参考答案:(1)0.2mol? 1.12L(2)361.8g
本题解析:
试题分析:(1)7.8g Na2O2的物质的量n=7.8/78=0.1mol,则根据方程式中的系数比例,可以求出氢氧化钠的物质的量也为0.1mol,氧气的物质的量为0.05mol,所以其体积为0.05*22.4=1.12L。
(2)最后Na+的物质的量为0.2mol,则水的物质的两0.1为20mol,加上反应消耗的水0.1mol,则总的水为20.1mol,质量为20.1*18=361.8g。
点评:本题考查化学方程式的计算,题目难度不大,注意开始时所用水的质量为消耗的质量和剩余水的质量
本题难度:一般
2、选择题 有两种体积相同的某植物的营养液,其配方如下表所示:
| KCl
| K2SO4
| ZnSO4
| ZnCl2
|
1
| 0.3mol
| 0.2mol
| 0.1mol
| -
|
2
| 0.1mol
| 0.3mol
| -
| 0.1mol
对于两种营养液的成分,下列说法中,正确的是( )
A.只有n(K+)相同 B.只有n(Cl-)相同
C.各离子的物质的量均不同 D.各离子的物质的量宪全相同
参考答案:D
本题解析:
试题分析:K离子的物质的量都是0.7mol,Cl离子的物质的量都是0.3mol, Zn离子的物质的量都是0.1mol, SO4离子的物质的量都是0.3mol,故D正确。
考点:物质的量的知识点。
本题难度:一般
3、选择题 已知1.505×1023个X气体分子的质量为8g,则X气体的摩尔质量是
A.16g
B.32g /mol
C.32g
D.64g /mol
参考答案:B
本题解析:1.505×1023个X气体分子的物质的量为0.25mol,则X气体的摩尔质量是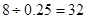 ?g /mol ?g /mol
本题难度:简单
4、选择题 设NA为阿伏加德罗常数,下列叙述中正确的是(?)
A.标准状况下,1.12L的SO3所含的原子数约为0.2NA
B.1 mol Na2O2中所含的阴离子数约为2NA
C.S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2NA
D.1L0.1mol·L-1Na2CO3溶液中含有0.1NA个CO32—
参考答案:C
本题解析:标准状况下,三氧化硫不是气体,不能适用于气体摩尔体积,A不正确;过氧化钠中阳离子和阴离子的个数之比是2︰1,所以选项B中所含的阴离子数约为NA;S2和S8都是S元数的不同单质,6.4g混合物中含有0.2molS原子,C正确;碳酸钠在溶液中CO32-水解,所以D中含有的CO32—个数小于0.1NA,D不正确,答案选C。
本题难度:一般
5、选择题 将一定量的CO2缓慢地通入500ml NaOH溶液中,充分反应后将溶液低温蒸发,得到不含结晶水的白色固体A 9.50g。取3份质量不同的A,分别与100ml相同物质的量浓度的盐酸反应,得到的气体体积(标准状况)与A的质量关系如下表所示:(???)
组别
| I
| II
| III
| 盐酸体积/ml
| 100
| 100
| 100
| A的质量/g
| 1.90
| 3.42
| 3.80
| 气体的体积/ml
| 448
| 716.8
| 672
下列说法不正确的是
A.第I组样品盐酸有剩余
B.若加入0.38g样品,则最终放出气体67.2mL
C.原NaOH的物质的量浓度是0.3mol·L—1
D.盐酸的物质的量浓度的0.5mol/L
参考答案:B
本题解析:
试题分析:B项:经分析,物质A应为Na2CO3与NaHCO3的混合物,因为盐酸要先跟Na2CO3反应生成NaHCO3,再与NaHCO3反应生成,故最终气体的体积少于,故不正确;故选B。
点评:本题考查混合物的计算,题目难度中等,本题注意对表中数据的分析,考查学生的数据分析能力,做题中注意讨论法的应用。
本题难度:一般
|
|