微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (10分)(1)在质量分数为28%的KOH水溶液中,OH-离子与H2O分子数之比是_______。
(2)在KCl和CaCl2所组成的某混合物中,K+与Ca2+的物质的量之比为2∶1,则该混合物中含CaCl2的质量分数为__________,KCl与CaCl2的物质的量之比为__________,含1 mol Cl-的该混合物的质量是____________g。
(3)在标准状况下,由CO和CO2组成的混合气体13.44 L,质量为20 g,该混合气体中,碳与氧两种原子的数目之比为__________。
参考答案:(1)5∶4
(2)42.7%? 2∶1? 86.7<
本题解析:(1)分别求出KOH和H2O的质量,转换成物质的量。
(2)混合物的物质的量比n(KCl)∶n(CaCl2)=2∶1再细分项计算。
(3)设CO、CO2分别为x mol,y mol
(x+y)×22.4="13.44?????????????????????????????????????????????????????????????" ①
(28x+44y)="20???????????????????????????????" ??????????????????????????????????②
再求(x+y)/(x+2y)=3∶4。
本题难度:简单
2、选择题 下列气体不可以用浓硫酸干燥的是
A.H2
B.NH3
C.SO2
D.Cl2
参考答案:B
本题解析:浓硫酸具有强氧化性及酸性,所以常温下还原性较强气体(例如HI)及碱性气体(例如氨气)不能用其干燥,答案为B
本题难度:一般
3、选择题 CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是(?)
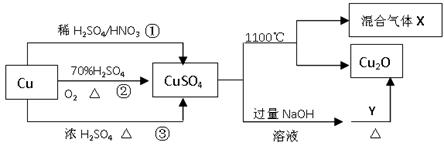
A.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3∶2
B.相对于途径①、③,途径②更好地体现了绿色化学思想
C.1molCuSO4在1100℃所得混合气体X中O2一定为0.75mol
D.Y可以是葡萄糖
参考答案:C
本题解析:
试题分析:1molCuSO4在1100℃所得混合气体X为SO2,O2,其中存在可逆反应SO2+O2 SO3,O2不一定为0.75mol4的制备
SO3,O2不一定为0.75mol4的制备
点评:本题考查CuSO4的制备,做题时,应注意框图之间各物质的联系,利用可逆反应的特征来解题。考查学生的综合能力,难度一般。
本题难度:简单
4、实验题 水蒸气通过灼热的煤所产生的混合气,其主要成份是CO、H2,还含有CO2和水蒸气请用下列装置设计一个实验,如图以确认上述混合气中含有CO和H2。

(1)连接上述装置的正确顺序是:(填各接口的代码字母)
混合气→(???)(???)接(???)(???)接(???)(???)接(???)(???)接(???)(???)。
(2)确认混合气中有H2的实验现象是______;
其理由是_______________。
参考答案:(1)混合气→(E)(F)接(D)(C)接(A)(B)接(J
本题解析:完全仪器连接的关键有三点;①在H2和CO还原CuO之前,应将混合气中的CO2和水蒸气除去,以防对后面实验的干扰,应先吸收CO2(可用NaOH溶液),而后再吸收水分(防止吸收CO2所用的NaOH溶液中有水蒸气带出,不能完全除去水);②吸收CO2最好用NaOH溶液,吸收完全,确认CO2的生成最好用石灰水(得到浑浊物便于观察);③H2、CO还原CuO后确认氧化产物H2O和CO2时,首先确定水蒸气,而后确定CO2。
本题难度:一般
5、实验题 下图所示装置可用来制取Fe(OH)2和观察Fe(OH)2在空气中被氧化时的颜色变化。实验时必须使用铁屑、6 mol/L H2SO4溶液和NaOH溶液。填写下列空白:
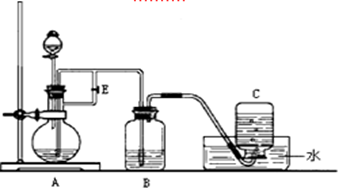
(1)B中盛有一定量的??????????????,A中应预先加入的试剂是?????????,A中反应的化学方程式为????????????????????????????????????????。
(2)实验开始时应先将活塞E???????(填“打开”或“关闭”),目的是??????????????????????????????????。
(3)A反应一段时间后将活塞E???????(填“打开”或“关闭”),目的是???????
????????????????????????????????????。
(4)实验结束,拔去装置B中的橡皮塞,使空气进入,Fe(OH)2被氧化。若反应过程中转移了0.04mol电子,则参加反应的氧气的体积为?????????L(标准状况)。
参考答案:(1)NaOH溶液?铁屑?? Fe+H2SO4===FeSO
本题解析:制取Fe(OH)2的关键是防止氧气的氧化,预先排除装置中的空气,结合所给装置及药品,制取Fe(OH)2:FeSO4+2NaOH=Fe(OH)2↓+Na2SO4;而通过反应Fe+H2SO4=FeSO4=H2↑产生的氢气来排除装置中的空气;
(1)检验装置气密性后,在A烧瓶中放入铁屑,分液漏斗中装有稀硫酸,B中盛放NaOH溶液
(2)实验开始时应先将活塞E打开,打开分液漏斗的活塞,产生氢气,让生成的氢气排走装置和溶液中的空气
(3)A反应一段时间后将活塞E关闭,继续产生的氢气使烧瓶内压强增大,把A中FeSO4溶液压入B中反应,与其中的NaOH溶液反应生成白色Fe(OH)2沉淀;
(4)实验结束,拔去装置B中的橡皮塞,使空气进入,Fe(OH)2被氧化,沉淀颜色由白迅速置换为灰绿色,最终转变为红褐色,完成实验
由4Fe(OH)2+O2+2H2O=4Fe(OH)3可知,反应中有4个电子的转移,当反应过程中转移了0.04mol电子,则参加反应的氧气为0.01mol,标准状况下体积为0.224L
本题难度:简单