微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 某学生拟用50mLNaOH溶液吸收CO2气体,制备Na2CO3溶液。为了防止通入过量CO2气体而生成
NaHCO3,他设计了如下实验步骤:
①取25mLNaOH溶液吸收过量的CO2气体,至CO2气体不再有
②小心煮费溶液1~2分钟排出溶液中溶解的CO2气体
③将得到的溶液中加入另一半(25mL)NaOH溶液,使溶液充分混合。

(1)能否制得较纯净的Na2CO3_________________理由是_________________
(2)按他的设计,第1步实验装置如图
①装置A中的离子反应方程式_________________
②装制B中的试剂是_________________作用是_________________
③有人认为实验步骤由②③的顺序对调,即先混合,再煮费,更合理,你认为对吗?_________________
(填合理或不合理),为什么?_________________。
2、实验题 硫代硫酸钠(Na3S2O3,在酸性溶液中不能稳定存在)可由亚硫酸钠和硫粉通过化合反应制得。装置如图I:有关物质的溶解度曲线如图Ⅱ所示。
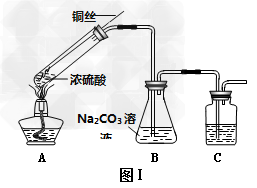
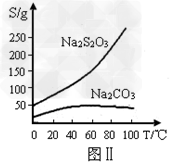
(1)Na3S2O3・5H2O的制备:???
①写出试管内发生反应的化学方程式___________。
②B中混合液被气流搅动,反应一段时同后.硫粉的量逐渐减少。当B中溶液的pH接近7时就停止加热,理由是________________;装置C的作用是_______________。????
③过滤B中的混合液,将滤液经过___________、____________、过滤、洗涤、烘干,得到产品。
(2)饱和Na2CO3溶液吸收少量SO2后所得溶液呈弱碱性。含有OH-、SO32-、HCO3-等阴离子。请设计试验方案,证明“滤液”中存在SO32-、HCO3-,写出实验步骤、预期现象和结论。???
? 限选仪器及试剂:pH计、小烧杯、试管、带塞导气管、滴管、玻璃棒、过滤装置和滤纸;2 mol・L-1、1 mol・L-1 BaCl2溶液、l mol・L-1Ba(NO3)2溶液、品红溶液、紫色石葛蕊试液、澄清石灰水等。
3、实验题 某化学兴趣小组用如下装置模拟工业制备造纸原料BaSO3,并测定产品纯度。
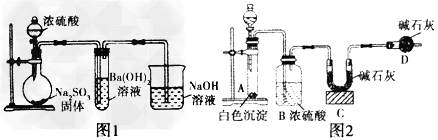
(1)图1烧瓶中发生反应的化学方程式为______________________________
(2)甲同学观察到图1试管中出现白色沉淀,该白色沉淀可能含有①BaSO3;②_________________________
(3)为探究白色沉淀的成分设计如下实验方案:

(4)为测定产品纯度取白色沉淀wg于图2装置的试管,在分液漏斗中加入____________(可从稀盐酸、稀硝酸、稀NaOH溶液中选择一种)。实验后,测得C装置增重mg,根据此实验数据可计算出白色沉淀中BaSO3的质量分数为__________(用含m、w的式子表示)。本测定方案有缺陷,请指出本方案的缺点及其对实验结果的可能影响 ________________________________________________
(5)为制备纯净的BaSO3,请设计改进图1装置的实验方案____________________。
4、推断题 实验室以含有Ca2+、Mg2+、Cl-、SO42-、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,流程如下:
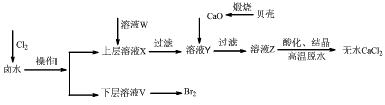
(1)操作I使用的试剂是_______________,用主要仪器的名称是_____________。
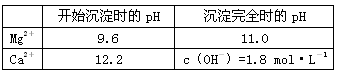
(2)加入溶液W的目的是___________________,用CaO调节溶液Y的pH,可以除去Mg。由表中数据可知,理论上可选择的pH最大范围是___________。酸化溶液Z时,使用的试剂为_____________。
(3)实验室用贝壳与稀盐酸反应制备并收集CO气体,下列装置中合理的是_____________________。
a.
b.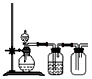
c.
d.
(4)常温下,H2SO3的电离常数K=1.2×10-2,,K=6.3×10-3;H2CO3的电离常数K=4.5×10-7,K=4.7×10-11某同学设计实验验证H2SO3酸性强于H2CO3;将SO2和CO2气体分别通入水中至饱和,立即用酸度计测两溶液的pH,若前者的pH小于后者,H2SO3酸性强于H2CO3,该实验设计不正确,错误在于_____________________。设计合理试验验证H2SO3酸性强于H2CO3(简要说明试验步骤、现象和结论)______________________________________。仪器自选。供选择的试剂:CO2、SO2、Na2CO3、NaHCO3、NaHSO3、蒸馏水、饱和石灰水、酸性KMnO4溶液、品红溶液、pH试纸。
5、实验题 硫酸铁(PFS)是一种新型高效的无机高分子絮凝剂, 广泛用于水的处理,用铁的氧化物为原料来制取聚合硫酸铁,为控制水解时Fe3+ 的浓度,防止生成氢氧化铁沉淀,原料中的Fe3+必须先还原为Fe2+ 。
实验步骤如下:

(1)用98%的硫酸配制28%的硫酸,所需的玻璃仪器除量筒外,还有_________。
a. 玻璃棒 b.烧杯 c.烧瓶
(2)步骤Ⅱ取样分析溶液中Fe2+ 、Fe3+的含量,目的是_______和确定氧化Fe2+所需NaClO3的量:
a. 控制溶液中Fe2+与Fe3+含量比
b. 确保铁的氧化物酸溶解完全
c. 确定下一步还原所需铁的量
(3)完成步骤Ⅳ中的氧化还原反应:补充产物并配平:
_____Fe2+ +____ClO3-+_____H+=_____Fe3+ +______Cl-+______
(4)聚合硫酸铁溶液中SO42-与Fe3+物质的量之比不是3:2。根据下列提供选 择的试剂和基本操作,测定聚合硫酸铁产品溶液中SO42-与Fe3+物质的量之比。 测定时所需的试剂____。
a.NaOH b.FeSO4 c.BaCl2 d.NaClO3
需要测定Fe2O3和____的质量(填写化合物的化学式)。