微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (16分)石墨在材料领域有重要应用。某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质。设计的提纯和综合应用工艺如下:
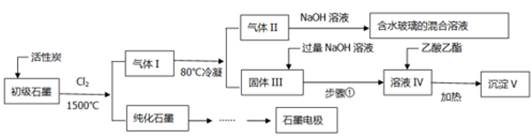
(注:SiCl4的沸点是57.6?C,金属氯化物的沸点均高于150?C)
(1)向反应器中通入Cl2前,需通一段时间的N2,主要目的是??????????????????????。
(2)高温反应后,石墨中的氧化物杂质均转变为相应的氯化物。气体I中的氯化物主要为??????????????????????。由气体II中某物质得到水玻璃的化学方程式为??????????????????????。
(3)步骤①为:搅拌、???????。所得溶液IV中阴离子有??????????????????????。
(4)由溶液IV生成沉淀V的总反应的离子方程式为??????????????????????。100kg初级石墨最多可获得V的质量为kg??????????????????????。
(5)石墨可用于自然水体中铜件的电化学防腐,完成下图防腐示意图,并作相应标注。
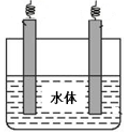
参考答案:(1)排除空气,减少C的损失;
(2)SiCl4+6N
本题解析:
试题分析:(1)石墨的化学性质在常温下稳定,而在高温下可与氧气发生反应,所以通入N2目的是作保护气,排除空气中的氧气,减少C的损失;
(2)高温反应后,石墨中的氧化物杂质均转变为相应的氯化物。根据杂质的含量,气体I中的氯化物主要SiCl4、AlCl3、FeCl3;SiCl4的沸点是57.6?C,所以气体II为SiCl4,与氢氧化钠溶液反应生成硅酸钠和氯化钠,化学方程式为SiCl4+6NaOH =Na2SiO3+4NaCl+3H2O;
(3)金属氯化物的沸点均高于150?C,所以固体II
本题难度:一般
2、选择题 向某天然硬水中加入石灰,离子方程式正确但不能降低水的硬度的是
A ?2Ca2++ 2HCO3-+2OH-=2CaCO3+2H2O
B? 2Ca2+ + Mg2++ 2HCO3-+4OH-=2CaCO3+2H2O+Mg(OH)2
C? 2OH-+ Mg2+= Mg(OH)2
D? CaCO3+H2O+CO2 = Ca2++ 2HCO3-
参考答案:C
本题解析:略
本题难度:一般
3、填空题 现有0.1mol・L-1的Na2SO4和0.1mol・L-1的H2SO4混合溶液100mL,向其中逐滴加入0.2mol・L-1的Ba(OH)2溶液,并不断搅拌,使反应充分进行。
⑴当加入50mLBa(OH)2溶液时,发生反应的离子方程式为????????????????,所得溶液中的溶质是?????????,其物质的量浓度为?????????????mol・L―1;
⑵当溶液中沉淀量达到最大时,所加Ba(OH)2溶液的体积为?????mL,所得溶液中溶质?????????,则该溶质物质的量浓度为 ??????????mol・L-1。
参考答案:(12分)⑴ 2H++2OH-+Ba2++SO42―==Ba
本题解析:
试题分析:n(Na2SO4)=0.01mol,n(H2SO4)= 0.01mol,n(H+)= 0.02mol,n(SO42―)=0.02mol。
⑴n[Ba(OH)2]=0.01mol,n(OH-)=0.02mol,n(Ba2+)=0.01mol。
发生的离子方程式为2H++2OH-+Ba2++SO42―==BaSO4↓+2H2O。由化学反应中量的关系可知,H+、OH-、Ba2+反应完,SO42―没反应完,Na+没参加反应,故所得溶液中的溶质是Na2SO4。其物质的量浓度为c=n÷V
本题难度:一般
4、选择题 下列离子方程式正确的是( )
A.向苯酚钠溶液中通入少量的CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32-
B.Ca(HCO3)2溶液中加入过量澄清石灰水:Ca2++HCO3-+OH-=CaCO3↓+H2O
C.铝与氢氧化钠溶液反应:Al+2OH-=AlO2-+H2↑
D.向KHSO4溶液中滴入Ba(OH)2溶液使pH=7:SO42-+H++Ba2++OH-=BaSO4↓+H2O
参考答案:A.向苯酚钠溶液中通入少量的CO2的离子反应为C6H5O-+
本题解析:
本题难度:一般
5、选择题 下列离子方程式书写正确的是
A.金属铝溶于氢氧化钠溶液: Al+2OH-=AlO2-+H2↑
B.Cl2溶于水: Cl2+H2O=2H++Cl-+ClO-
C.Na2SO3溶液使酸性KMnO4溶液褪色:5SO32-+6H++2MnO4-=5SO42-+2Mn2++3H2O
D.NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O
参考答案:C
本题解析:A:反应物水没有写出:2Al+2OH-+2H2O=2AlO2-+3H2↑,不正确
B:产物次氯酸为弱电解质,不能拆为离子,不正确
C:正确
D:两溶液反应至中性则物质的量比为2:1,2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,不正确
本题难度:一般