微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 工厂的工业废水,不可直接往江河湖海中排放,否则会造成严重公害。某河道两旁有甲、乙两厂,它们排出的工业废水各含有K+、Fe3+、Ba2+、Ag+、Cl-、SO42-、NO3-、OH-中的四种。又知甲厂污水pH>7。
(1)甲厂污水中含有的四种离子可能是:_______________________________。
(2)乙厂污水中含有的四种离子可能是:______________________________。
(3)对乙厂废水进行处理,方法之一,可往废水中加入一定量的________(选填
“活性碳”“硫酸亚铁”或“铁粉”),可以回收其中的金属__________(填
元素符号)。
(4)消除污染的另一种重要措施是将甲、乙两厂的废水按比例混合,可使废水中的________(填离子符号)转化为沉淀,从而大大降低污染程度。过滤后所得废水主要含________,可用于浇灌农田。
参考答案:(1)OH-、Cl-、SO42-、K+
(2)Fe3+
本题解析:(1)(2)由甲厂废水pH>7知必有OH-,则与之不能大量共存的Fe3+、Ag+必须在乙厂废水中,由Ag+不能与Cl-、SO42-大量共存,知乙厂废水中必有NO3-,而SO42-必在甲厂废水中,则Ba2+又必在乙厂废水中,可将8种离子分开。
(3)乙厂废水含Fe3+、Ba2+、Ag+、NO3-,能与备选试剂反应得金属单质的只有Fe粉,可回收Ag。
(4)对比甲厂、乙厂废水中的离子,可看出混合能生成Fe(OH)3、AgCl、BaSO4沉淀,过滤后主要成分是KNO3,KNO3是一种化肥。
本题难度:一般
2、选择题 下列各组离子在强酸性溶液中能大量共存的是( )
A.Ba2+ Na+ SCN--- Fe3+
B.Mg2+ Cl-Al3+ SO42-
C.K+ Cl- HCO3- NO3-
D.Ca2+ Na+ Fe3+ AlO2-
参考答案:B
本题解析:在强酸溶液中HCO3-、AlO2-不能存在,SCN―与Fe3+反应,Fe3+与AlO2-发生双水解反应,能大量共存的是选项B。
本题难度:一般
3、选择题 酸碱指示剂一般是有机弱酸(用Hln表示)或弱碱,其分子形式与电离出的ln―形式颜色不同,在pH值不同的溶液中至所以能表现出不同的颜色,是因为其电离平衡发生移动的结果。甲基橙是一种常用的酸碱指示剂,溶于水后发生如下电离:Hln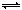 H++ln―,已知在pH<3.1的溶液中呈红色,在pH>4.4的溶液中呈黄色,下列判断中不正确的是?(???)
H++ln―,已知在pH<3.1的溶液中呈红色,在pH>4.4的溶液中呈黄色,下列判断中不正确的是?(???)
A.Hln呈红色
B.ln―呈黄色
C.遇pH值介于3.1~4.4的溶液可能呈橙色
D.Hln呈黄色
参考答案:D
本题解析:碱性溶液有利于平衡向右进行,使c(ln―)增大,而此时溶液变黄色,说明ln―呈黄色。
本题难度:简单
4、选择题 下列各组离子一定能在无色溶液中大量共存的是
A.Na+、CO32-、NO3-、AlO2-
B.K+、H+、CrO42-、SO32-
C.Al3+、Ba2+、HCO3-、Cl-
D.Fe3+、Mg2+、SCN-、Cl-
参考答案:A
本题解析:
试题分析:离子间如果发生化学反应,则不能大量共存,反之是可以的。A、Na+、CO32-、NO3-、AlO2-在无色溶液中大量共存,A正确;B、CrO42-与SO32-发生氧化还原反应,且H+与SO32-反应,CrO42-在溶液中不是无色的,B不正确;C、在溶液中Al3+和HCO3-在溶液中水解相互促进生成氢氧化铝和CO2,不能大量共存,C不正确;D、Fe3+和SCN-不能大量共存,D不正确,答案选A。
本题难度:一般
5、填空题 (1)物质的量浓度相同的三种盐NX、NaY、NaZ的溶液,其pH依次为8、9、1 0,则HX、HY、HZ的酸性由强到弱的顺序是???????????????????。
(2)比较下列溶液的pH(填“>”“<”或“=”):
①0.1 mol・L-1Na2CO3溶液????0.1 mol・L-1NaHCO3溶液
②0.1 mol・L-1NH4Cl溶液????0.01 mol・L-1NH4C1溶液
(3)把a、b、c、d四块金属片浸泡在稀H2SO4中,用导线两两相连,可以组成各种原电池。若a、b相连,a为负极;c、d相连,c为负极;a、c相连,c为正极;b、d相连,b为正极,则这四种金属的活动性由强到弱的顺序为 ??????????????。
(4)将AlCl3溶液蒸干、灼烧,最后所得的固体的主要成份是???????????。
(5)氯化铁溶液呈?????性(填“酸”、“碱”或“中”),原因是(用离子方程式表示):?????????????????????????????????????????????????????????????????
(6)向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-刚好沉淀完全时,溶液的pH???7(填“>”“<”或“=”),离子反应总方程式为:?????????????????????。
参考答案:
(1)HX>HY>HZ(2)>;< (3)a>c>d
本题解析:
试题分析:(1)因pH越大,说明酸根离子水解越是强烈,对应的酸越弱,所以HX、HY、HZ的酸性由强到弱的顺序:HX>HY>HZ
(2) ①同浓度的Na2CO3和NaHCO3溶液,CO32-水解程度大于 HCO3-所以0.1 mol・L-1Na2CO3溶液?> 0.1 mol・L-1NaHCO3溶液②不同浓度的NH4Cl溶液浓度越小,NH4+水解程度越大,但是水解后溶液的酸性越弱。所以②0.1 mol・L-1NH4Cl溶液 < 0.01 mol・L-1NH4C1溶液
本题难度:一般