微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列实验过程中产生的现象与对应图形相符合的是( )
A.
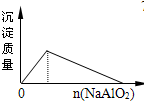
向盐酸中加入NaAlO2溶液
B.
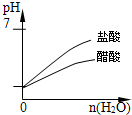
pH=1的醋酸和盐酸分别加等量水稀释
C.
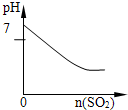
SO2气体通入溴水中
D.
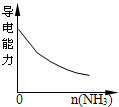
氨气通入醋酸溶液中
2、填空题 (18分)、现有下列物质:①H2S、②NH3、③H2SO4、④NaHCO3、
⑤CH3COOH、⑥KNO3溶液、⑦盐酸、⑧酒精、⑨二元酸H2A等。请回答下列问题(请填入序号)。
(1)其中一定属于弱电解质的是 。不能确定的是 ,请设计一个实验以证明它是强电解质还是弱电解质。你的实验和结论是
;
(2)H2S在水中的电离方程式为 __________;
NaHCO3在水中的电离方程式为 ;
 已知H2A的电离方程式为:H2A ="=" H++HA-; HA- H++A2-。试判断H2A是 电解质(填“强”或“弱”)。
已知H2A的电离方程式为:H2A ="=" H++HA-; HA- H++A2-。试判断H2A是 电解质(填“强”或“弱”)。
(3)2mol/L的盐酸和2mol/L的醋酸各100ml,分别与过量的Zn反应,生成H2的体积,V(盐酸) V(醋酸)(填>、=或<);氢离子浓度相等的盐酸和醋酸各100ml,分别与过量的Zn反应,生成H2的体积V(盐酸) V(醋酸) (填>、=或<);理由是
;
 (4)已知CH3COO-+H+ CH3COOH;现要使平衡向右移动且氢离子浓度增大,应采取的措施是( )
(4)已知CH3COO-+H+ CH3COOH;现要使平衡向右移动且氢离子浓度增大,应采取的措施是( )
A.加NaOH
B.加盐酸
C.加水
D.升高温度
已知CH3COOH在溶剂A中可以全部电离,盐不溶解于A溶剂。则CH3COOH在溶剂A中的电离方程式为 ;CH3COOH和Na2CO3在溶剂A中生成CO2反应的离子方程式是 。
3、选择题 将0.1mol/L的CH3COOH加水稀释,有关稀释后醋酸溶液的说法中,错误的是( )
A.电离程度增大
B.溶液中离子总数增多
C.溶液导电性增强
D.溶液中醋酸分子减少
4、选择题 物质的量浓度都为1mol/L的盐酸和醋酸各100 mL,分别加入5g锌粉,在相同条件下充分反应,有关叙述正确的是
[ ??? ]
A.醋酸与锌反应放出氢气多
B.盐酸和醋酸分别与锌反应放出的氢气一样多
C.醋酸与锌反应速率慢
D.盐酸和醋酸分别与锌反应的速率一样大
5、填空题 已知:
酸
| 电离常数(Ka)
| 酸
| 电离常数(Ka)
|
CH3COOH
| 1.8×10-5
| HCN
| 5×10-10
|
H2CO3
| Ka1 =" " 4.2×10-7
| HClO
| 3×10-8
|
Ka2 =" " 5.6×10-11
(1)用方程式表示HCN溶液显酸性的原因:______________________________。
(2)上述四种酸中,酸性最强的是 ;
(3)25℃时,0.01 mol/L NaCN溶液的pH________7;
(4)在浓度均为0.01 mol/L的CH3COONa、NaClO、Na2CO3的混合溶液中,逐滴加入0.01 mol/L HCl,则体系中酸根离子反应的先后顺序为 ;
(5)向pH=4的CH3COOH溶液中,加入下列物质,能使CH3COOH电离平衡向逆向移动的是:_________________。
①加入少量NH4Cl固体 ②加入等体积pH=5的盐酸
③加入少量Na2CO3固体 ④加入等体积0.01 mol/L的CH3COONa 溶液
|