微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 海水中可提取多种化工原料,下面是工业上对海水的几项综合利用示意图。
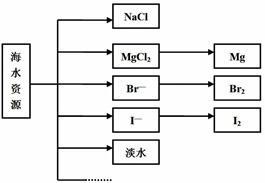
按要求回答问题:
(1)浩瀚的海洋是一个巨大的宝库,蕴含有80多种元素,可供提取利用的有50多种。下列物质不需要通过化学变化就能够从海水中获得的是??????。
A.食盐??????B.金属钠??????C.淡水
(2)以电解食盐水为基础制取Cl2、??????等产品的工业称为“氯碱工业”。
(3)实验室制取氯气的反应原理为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气????
MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气????
(填写装置的序号)。

(4)实验室中模拟Br―→Br2的转化,可以通过在KBr溶液中滴加少量新制氯水的实验进行实现。写出Br―→Br2的转化离子方程式为:??????;氯水不稳定,要现用现配,下列吸收氯气制备氯水的装置最合理的是??????(选填下列选项的编号字母)。
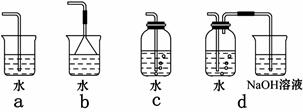
(5)电解熔融氯化镁所得的镁蒸气冷却后即为固体镁。下列气体中,镁蒸气可以在其氛围中冷却的是 ?? (选填下列选项的编号字母)。
A.Cl2 B.N2 C.Ar D.空气 E.H2
参考答案:(12分)(1)AC? [2分,答对一个给1分,有错不给分]
本题解析:
试题分析:(1)海水蒸发浓缩即可以得到食盐。另外海水淡化也是物理变化,金属钠的制备需要通过电解发获得,答案选AC。
(2)以电解食盐水为基础制取Cl2、氢气和氢氧化钠等产品的工业称为“氯碱工业”。
(3)根据反应的化学方程式可知,该反应是固体和液体之间需要加热得到气体的,所以应该选择的装置是b。
(4)氯气具有强氧化性,能把溴离子氧化生成单质溴,则反应的离子方程式是2Br― + Cl2= 2Cl― + Br2。由于氯气在水中的溶解度不大,所以没有必要防止倒吸,但氯气有毒,需要尾气
本题难度:一般
2、选择题 砹(At)是核电荷数最大的卤族元素,试推测砹及其化合物最不可能具有的性质是
A.单质砹易溶于某些有机溶剂
B.HAt受热很难分解
C.AgAt是不溶于水的有色固体
D.KAt的熔、沸点较高
参考答案:B
本题解析:根据卤素的性质递变可推之.I2、Br2易溶于有机溶剂,At2也易溶于有机溶剂;还原性HF<HCl<HBr<HI,由此知HI<HAt,因此HAt受热易分解,AgCl、AgBr、AgI难溶,AgAt难溶,KCl、KBr、KI熔、沸点较高,KAt也较高.
本题难度:简单
3、实验题 (8分)为测定Cl2、Br2的氧化性强弱,设计了如下实验:
(可供选择的试剂有:氯水、溴水、NaCl溶液、NaBr溶液、酒精、四氯化碳)
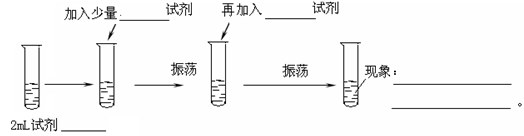
实验步骤如下:
由上回答下列问题:
(1)2ml试剂是?????????,加入少量?????????试剂,再加入?????????试剂
(2)现象是??????????????????????????????????????????????????????????。
(3)此实验可以证明Cl2的氧化性???????(填强于、弱于)Br2的氧化性,此反应
的离子反应方程式为:???????????????????????????????????????????????。
参考答案:(1)NaBr溶液、氯水、四氯化碳
(2)溶液分层,下
本题解析:要想证明氯气的氧化性强于单质溴的,可以利用单质间的相互置换能量来进行。因此可想溴化钠人员占和加入少量的氯水,反应后如果再加入四氯化碳,下层溶液如果显红棕色就能证明有单质溴生成。
本题难度:一般
4、选择题 7.1克氯气与下列金属完全反应时,消耗金属质量最多的是( )
A.铝
B.铁
C.镁
D.钠
参考答案:A、2Al+3Cl2=2AlCl3,Al~Al3+~3e-;
本题解析:
本题难度:一般
5、选择题 三氯化氮分子中每个原子的最外层均达到8电子稳定结构,且氮与氯的共用电子对偏向氮原子。则下列关于三氯化氮的叙述正确的是(??? )
A.NCl3为非极性分子
B.NCl3跟水反应的产物为NH3和HClO
C.NCl3跟水反应生成NH4Cl、O2和Cl2
D.在NCl3分子中N为+3价,跟水发生水解反应的产物是HNO2和HCl
参考答案:B
本题解析:因氮与氯的共用电子对偏向氮原子,则在NCl3中,N显-3价,Cl显+1价,则其发生水解的方程式应为:NCl3+3H2O====NH3+3HClO。又因氨气分子的空间构型推知NCl3为三角锥形结构,为极性分子。
本题难度:简单