微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 己知NH3极易溶于水,而难溶于有机溶剂四氯化碳。下列装置不适宜做NH3尾气吸收的是(???)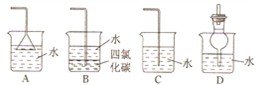
参考答案:C
本题解析:考查气体的吸收及实验安全。氨气极易溶于水,如果直接插入水中液体容易倒流,实验吸收氨气时必须防止液体倒流,选项AD都是正确的操作。由于氨气不溶于四氯化碳中,且四氯化碳的不溶于水,密度大于水,所以选项B也是可以防倒吸的,选项C不能,答案选C。
本题难度:一般
2、实验题 钴(Co)的氧化物是一种重要的化工原料,工业上利用CoCO3+O2→CoxOy+ CO2反应来生产相应的钴的氧化物。实验室中可以用下列装置来制取钴的氧化物并测定其分子组成。
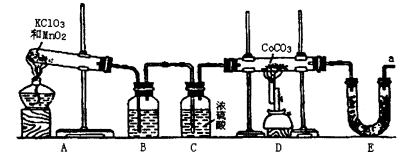
请填写下列空白:
(1)写出A装置的大试管里发生反应的化学方程式?????????????????????;
(2)E装置的U形管里盛放的物质是?????????????;
A.P2O5???????B.无水CaCl2???????C.碱石灰???????D.无水CuSO4
(3)O3的氧化性比O2强。已知制得的O2中含有少量的Cl2和O3,则B装置中所盛放的物质是??????????????????
A.NaOH溶液??? B.饱和NaHCO3溶液??? C.饱和NaCI溶液 ??D.KI溶液
(4)实验结束时,若先撤去A装置中的酒精灯,会引起???????????????;
(5)在CoCO3完全转化为CoxOy后,若称得E管增重4.40g,D管内残留物质的质量是8.30g,则生成CoxOy的化学式为??????????????????????;
(6)此实验装置存在一个比较大的缺陷,如何完善???????????????????。
参考答案:(1) 2KClO3 本题解析:
本题解析:
试题分析:由装置图可知,实验通过测定装置E中的增重,确定生成的二氧化碳的质量,再利用n(C)=n(Co)可知CoxOy中Co的物质的量,进而计算Co的质量。装置D管内残留物质是CoxOy,计算出氧元素质量,再计算氧原子的物质的量,根据原子物质的量之比确定化学式。
(1)在二氧化锰作催化剂,加热条件下,氯酸钾分解生成氯化钾、氧气,反应的化学方程式为2KClO3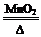 2KCl+3O2↑。
2KCl+3O2↑。
(2)E装置的U形管里盛放的物质用于吸收装置D生成的二氧化碳。A、P2O5;B、无水CaCl2;D、无水CuSO4均不能吸收二氧化碳。C、碱石灰是碱性干燥剂,可以吸收二氧化碳,故装置E中试剂为碱石灰,所以答案选C。
(3)制得的O2中含有少量的Cl2和O3,B装置中所盛放的物质用于吸收Cl2和臭氧。A、NaOH溶液可以吸收氯气,但不能吸收臭氧,所以A不正确;B、饱和NaHCO3溶液以吸收氯气,但生成二氧化碳,影响二氧化碳质量的测定,且不能吸收臭氧,故B不符合;C、饱和NaCl溶液不能吸收氯气和臭氧,故C错误;D、KI溶液吸收氯气和臭氧,所以D符合,答案选D。
(4)实验结束时,若先撤去A装置中的酒精灯,会导致装置A中的压强降低,容易发生倒吸。
(5)E管增重4.40g是二氧化碳的质量,物质的量为4.40g÷44g/mol=0.1mol。根据化学式CoCO3可知n(Co)=n(C)=0.1mol,则Co的质量为0.1mol×59g/mol=5.9g。D管内残留物质的质量8.30g是CoxOy的质量,CoxOy中氧元素质量为8.30g-5.9g=2.4g,氧原子的物质的量n(O)=2.4g÷16/mol=0.15mol,所以n(Co):n(C)=0.1mol:0.15mol=2:3,即该钴的氧化物的化学式为Co2O3。
(6)由于装置E中碱石灰也可以吸收空气中水蒸气、二氧化碳,影响二氧化碳质量的测定,因此应在a处接一装有碱石灰的干燥管,吸收空气中水蒸气、二氧化碳,防止进入装置E中。
本题难度:一般
3、选择题 下图所示装置是化学实验室的常用装置,它有多种用途.以下各项用途和操作都正确的是
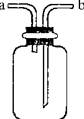
A.干燥CO2:瓶内放一定体积浓硫酸,由a进气
B.用于收集O2:瓶内充满水,由b进气
C.提供少量CO:瓶内充满CO,b接进水管
D.用做H2S和SO2反应的装置:由a通入H2S,b通入SO2
(已知:2H2S+SO2=3S+2H2O)
参考答案:C
本题解析:略
本题难度:简单
4、填空题 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯。回答下列问题:
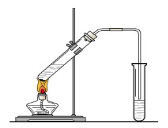
(1)写出制取乙酸乙酯的化学反应方程式: ??????????????????? ????。
(2)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法(加入试剂顺序)是:????????????????????????????????????????????????????????????。
(3)浓硫酸的作用是:①??????????????????;②???????????????????。
(4)饱和碳酸钠溶液的主要作用是???????????????????????????????????????????????????????????
?????????????????????????????????????????????????????。
(5)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止????? 。
(6)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 ????????
参考答案:(1) 本题解析:
本题解析:
试题分析:(1)在催化剂的作用下,乙酸和乙醇发生酯化反应生成乙酸乙酯,则该反应的化学方程式是 。
。
(2)由于浓硫酸的密度大于水的,且溶于水放热。又因为乙醇和乙酸都是挥发性的,所以加入试剂的先后顺序是先加乙醇,再缓慢滴加浓硫酸,最后滴加乙酸。
(3)在反应中浓硫酸起到催化剂的作用。又因为该反应是可逆反应,且有水生成,所以浓硫酸还起到吸水剂的作用。
(4)由于生成的乙酸乙酯中含有乙醇和乙酸,且乙酸乙酯不溶于水,所以饱和碳酸钠溶液的作用是中和乙酸,溶解乙醇,降低乙酸乙酯的溶解度,便于析出乙酸乙酯。
(5)由于生成的乙酸乙酯中含有乙醇和乙酸,而乙酸和乙醇与水都是互溶的,乙醇不能插入到溶液中的原因是防止倒吸。
(6)由于乙酸乙酯不溶于水,所以若要把制得的乙酸乙酯分离出来,应采用的实验操作是分液。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生实验能力的培养和解题方法的指导与训练,有助于培养学生规范、严谨的实验设计能力。该类试题主要是以实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。
本题难度:一般
5、实验题 用一种试剂除去下列各气体中的杂质(括号内为杂质):
(1)CO2(SO2):试剂 ,离子方程式 ????????
(2)SO2(HCl):试剂 ,离子方程式 ?????? ?
参考答案:(1)溴水 ,离子方程式 Br2 + 2H2O + SO2
本题解析:略
本题难度:简单