��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ������ʵ���������ÿ�����þ��Ϊԭ����ȡ��������þ(Mg3N2)����֪ʵ���п��ܻᷢ�����з�Ӧ��
��2Mg+O2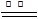 2MgO����3Mg+N2
2MgO����3Mg+N2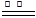 Mg3N2����2Mg+CO2
Mg3N2����2Mg+CO2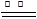 2MgO+C��
2MgO+C��
��Mg+H2O MgO+H2���� ��Mg3N2 +6H2O
MgO+H2���� ��Mg3N2 +6H2O 3Mg(OH)2+2NH3��
3Mg(OH)2+2NH3��
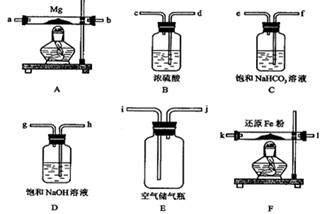
�ɹ�ѡ���װ�ú�ҩƷ����ͼ��ʾ(þ�ۡ���ԭ���۾��Ѹ��װ�����������ķ�Ӧ����ȫ�ģ�����װ�õ�ĩ������������)��
�ش��������⣺
��1�������ʵ�鷽��ʱ����װ��A��D��E�⣬��Ӧѡ���װ����????????????������ĸ���ţ���ѡ��װ��DĿ��Ϊ_____________________________???????????????????????????��
��2��ͨ����Ӧ�ȵ�ȼ????????���ľƾ��ƣ����ͬʱ��ȼA��Fװ�õľƾ��ƣ�����ʹʵ����???????????���ƫ�ߡ���ƫ�͡���ԭ��????????????????????????????????????????????????
��3�������һ��ʵ�飬��֤������Mg3N2��д���������衢����ͽ��ۣ�
_____________________________________________________________________??????????
�ο��𰸣���1��BF?��2�֣�?? D Ŀ���dz�ȥ�����е�CO2������
���������
�����������1���÷�Ӧ��Ϊ�˵õ������ĵ���þ�������Ӱ��IJ��������ˮ����������ȥ����װ��B��������ȥˮ�����ģ�����A֮ǰ��F����������ȥ������D Ŀ���dz�ȥ�����е�CO2�����ⷴӦ�۷�����
��2����һװ���У��ܶ��˿��ܻῼ�ǵ�Fװ����������ȥˮ�����ģ������Ļ�����Ӧ������������ô�죬������װ����������ȥ�����ġ����װ��F�еĻ�ԭ����û�дﵽ��Ӧ�¶�ʱ���������ܳ�����������ͬþ��Ӧ����ʹ����þ�л�������þ����2�֣�
��3����֤������Mg3N2���������õ���þ��������Ӧ��ȡ������������Թ��У��μ�����ˮ������ʪ�ĺ�ɫʯ����ֽ�����Թܿڣ�����Թ��е���Һ���ֻ��ǣ���ɫʯ����ֽ�����������֤���е���þ���ɡ�
�����Ѷȣ�һ��
2��ʵ���� ��������ҽҩ��ʯ����ҵ���й㷺��;����ͼ��ģ�ҵ�Ʊ�������ֲ�Ʒ�����Ƶ����̣�
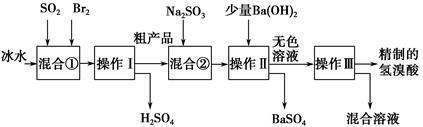
�����������̻ش��������⣺
(1)��Ϣ��з�����Ӧ�����ӷ���ʽΪ________________________________��
(2)��Ϣ���ʹ�ñ�ˮ��Ŀ����_______________________________________��
(3)������һ�������ڷ���________����(�����)
a�������Һ��? b���������
c���������ܵ�Һ��? d�����ܵ�Һ��
(4)��Ϣ��м���Na2SO3��Ŀ����____________________________________��
(5)������������ӦΪ��ɫҺ�壬��ʵ�ʹ�ҵ�������Ƶõ�������(��ҵ������)���е����Ļ�ɫ�����Ǽ�����ͬѧ����˼�ʵ�����̽����
��ͬѧ���蹤ҵ������ʵ���ɫ����Ϊ���к���Fe3����������֤���ü������õ��Լ�Ϊ________������������ɹ۲쵽������Ϊ__________________����ͬѧ���蹤ҵ������ʵ���ɫ����Ϊ���к���________________��������֤���ü������õ��Լ�Ϊ____________��
�ο��𰸣�(5)KSCN��Һ����Һ��ɺ�ɫ��Br2��CCl4(��������
���������SO2��Br2��ˮ�з���������ԭ��Ӧ����Ӧ���ȣ�Ϊ��ֹ���������ñ�ˮ���¡�������������������ǹ��ˡ���Ϣ��м���Na2SO3��Ŀ���dz�ȥ�ֲ�Ʒ��δ��Ӧ����塣����Fe3������KSCN��Һ����ҵ�������п��ܺ�������ʵ���ɫ���������Ȼ�̼��ȡ��֤����
�����Ѷȣ�����
3������� ͼ���ǻ�ѧʵ�����г����Ʊ�����������IJ�������װ�ã�ijѧУͬѧ������ѧ�����Լ��������������ʵ�飮
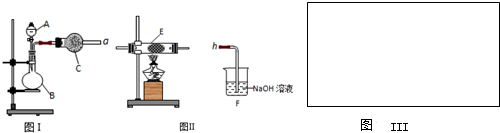
��1��ͼ��������B�����ƣ�______��
��2��ͬѧ������ͼ��װ���Ʊ����ռ������NO2���壬���ڷ����ڻ����ü���ƿ�ռ�NO2��װ��ͼ______��B�з�����Ӧ�����ӷ���ʽΪ______��
��3��ͬѧ������ͼ��װ��ͨ��������Ӧǰ��C��������ȷ��Na2CO3��NaCl����������Na2CO3��������A�м���ϡ���ᣬB�м���Na2CO3��NaCl�������C�м����ʯ�ң���װ�ô��ڽ϶�ȱ�ݣ��Ӷ�����ʵ�����ϴ�����˵�����е�����ȱ�ݣ�
��______��
��______��
��4��ͬѧ������ͼ��װ����ȡ�����������Ļ�����壬��������ͼ��װ����֤����ijЩ���ʣ�A�м���Ũ��ˮ��C�м����ʯ�ң�E�ڷ��ô�������ʯ�ޣ����������������Ӹ�����a��b��c��h��
��B�����������Լ�������Ϊ______��B���ܲ���������������������ԭ����______��
��ʵ���й۲쵽E���к���ɫ������֣�֤����������______�ԣ�E�з�����Ӧ�Ļ�ѧ����ʽΪ______��
�ο��𰸣���1��ͼ��������B��Բ����ƿ���ʴ�Ϊ��Բ����ƿ��
��
���������
�����Ѷȣ�һ��
4��ѡ���� ��NaCl��������0.1 mol��L-1��NaCl��Һ�����в�����˵����ȷ���ǣ�???��
A����5.85gNaCl��������1 Lˮ�п����0.1 mol��L-1��NaCl��Һ
B������ʱ���ӹ۲�Һ�棬ʵ����ƫ��
C�������ܽ����Һת�Ƶ�����ƿ�У�Ȼ��������ƿ��ֱ�Ӽ�ˮϡ�͵��̶���
D��������Һʱ����ƿ��ԭ������������ˮ����Ӱ��ʵ����
�ο��𰸣�BD
���������
���������A�1 Lˮ�������������Һ���������Һ�������ˮ�������������Һ���ܶȻ�С���ʴ���C�����Һת�Ƶ�����ƿ�У�Ҫ����������ƿ���ʴ�����ѡBD��
���������⿼�������Һ�����ơ�ѧ��Ҫ����ס�䲽�裬������ȷ�Ľ��������⡣
��1�����㣺������������������ʵ�������Һ��Ũ��Һ�������
��2����������������ƽ������������������Ͳ��Ӧ����Һ�ܣ�����ѧ��һ������Ͳ����ȡҺ�������
��3���ܽ⣺���ձ����ܽ��ϡ�����ʣ��ָ������£��粻����ȫ�ܽ���ʵ����ȣ����������ƿ�Ƿ�©ˮ
��4��ת�ƣ����ձ�����ȴ�����Һ�ز�����С��ת��һ�����������ƿ�У��������¶�Ӧ��������ƿ�̶������£���
��5��ϴ�ӣ�������ˮϴ���ձ��Ͳ�����2��3�Σ�����ϴ��Һת�������У���ʹ��Һ��Ͼ��ȡ�
��6�����ݣ�������ƿ�м�ˮ���̶�������1cm��2cm��ʱ�����ý�ͷ�ιܼ�ˮ��ʹ��Һ����ǡ����̶������С�
��7��ҡ�ȣ��Ǻ�ƿ������ʳָ��סƿ������һֻ�ֵ���ָ��סƿ�ף��������µߵ���ʹ��Һ��Ͼ��ȡ�
������ƺõ���Һ�����Լ�ƿ�У����ñ�ǩ��
Ӱ�죺
1.����ʱ������
2.δ���ձ�ϴ�ӣ�ʹ��Һ�����������٣�������ҺŨ�Ƚ��͡�
3.ת��ʱ��С�Ľ�����Һ������Ũ��ƫ�͡�
��ȫע�⣺
1.��������Ϊ���Ի�ѧ���ʣ�Ũ����Ϊ���Ի�ѧ���ʣ�ע�ⲻҪ�������ϡ����ϡ����ⸯʴ��
2.Ҫע������ȷ��
3.ע����Һ�ܵ�ʹ��
4.ϡ��Ũ�����ǰ������ˮ�У��ò��������衣
5.����ƿ��ʹ��ǰ�������Դ:91������ www.91eXam.org©����©�IJ���Ϊע������ˮ�����߸���,�Ǻ�ƿ��.������סƿ��,����2min���۲�ƿ���Ƿ���ˮ���粻©,��������ת180�ȣ��ټ�©.��©ˮ���軻һ������ƿ,�ټ�©��
6.��������ŨҺ��ϡ�Ͷ�������Һʱ������Ũ��������ϡ����ʱ����Ӧ��ϴ����������Ũ�������Ͳ����Ϊ��Ͳ����Ƶ�ʱ���Ѿ����ǵ�����ʣ��Һ����������������Һ���ʵ����Ĵ�С�����仯��
7.��ҺǰӦ��������Һ�¶Ȼָ������£����������ƹ�������ˮ���ȣ�Ũ����ϡ�ͷ��ȣ�����粒�������ˮ���ȣ��������������ƿ������������
�����Ѷȣ���
5��ѡ���� ʵ������ȡ��������ʱ������β�����շ����в���ȷ����
A��Cl2��β��������NaOH��Һ����
B��NH3��β��������H2SO4��Һ����
C��SO2��β������������KMnO4��Һ����
D��NO2���������H2O������
�ο��𰸣�D
���������
��:D
A ?Cl2��2NaOH=NaCl��NaClO��H2O
B? 2NH3��H2SO4=(NH4)2SO4
C? 5SO2��2MnO4�D��2H2O=5SO42�D��2Mn2����4H��
D?Ӧ��NaOH��Na2CO3��������
�����Ѷȣ�һ��