微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列反应类型中,可能应用到浓硫酸的催化吸水作用的是
A.加成反应
B.取代反应
C.消去反应
D.氧化反应
参考答案:B
本题解析:浓硫酸的催化吸水作用一般表现在取代反应中,如酯化反应、硝化反应等。
本题难度:困难
2、选择题 要除去MgCl2酸性溶液中少量的FeCl3,不宜选用的试剂是
A.MgO
B.MgCO3
C.NaOH
D.Mg(OH)2
参考答案:C
本题解析:将pH调节到3左右。如使用NaOH,pH过高导致镁离子沉淀。
本题难度:简单
3、实验题 (11分)某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:
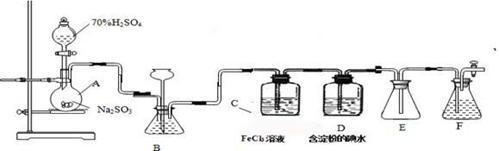
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若 ,则整个装置气密性良好。装置E的作用是 。装置F中为 溶液。
(2)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 。
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(3)SO2气体还原Fe3+反应的产物是________________(填离子符号)。
(4)在上述装置中通入过量的SO2为了验证C中SO2与Fe3+发生了氧化还原反应,他们取C中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去。
方案②:往第一份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是____ ,原因是_______________________________________。
(5)能表明I-的还原性弱于SO2的现象是__________________________,
写出有关离子方程式:
参考答案:(1)液柱高度保持不变 ;安全瓶,防止倒吸;NaOH(各1分
本题解析:
试题分析:(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若液柱高度保持不变,说明不漏气,则气密性良好;装置E的作用为:安全瓶,可防止液体倒吸;E中盛放NaOH溶液进行尾气处理,防止含硫化合物排放在环境中,从而保护环境。
(2)二氧化硫能溶于水生成亚硫酸,二氧化硫和亚硫酸钠、碳酸氢钠反应,为防止二氧化硫溶解,应该用亚硫酸氢钠溶液洗气,故选C。
(3)二氧化硫具有还原性、铁离子具有氧化性,二者发生氧化还原反应生成硫酸根离子和亚铁离子,
故答案为:Fe2+、SO42-。
(4)方案①往第一份试液中加入KMnO4溶液,紫红色褪去,原来溶液中有二氧化硫,二氧化硫和亚铁离子都能被酸性高锰酸钾溶液氧化而导致酸性高锰酸钾溶液褪色,所以不能确定哪种微粒其作用,故错误;方案②:往第一份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红,亚铁离子和KSCN不反应,铁离子和KSCN反应生成血红色溶液,所以可以检验溶液中存在亚铁离子,故正确;方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀,亚硫酸根离子和氯化钡不反应,硫酸根离子和钡离子反应生成硫酸钡沉淀,且不溶于稀盐酸,所以可以检验溶液中存在硫酸根离子,故正确;所以实验方案①不合理。
(5)SO2通入含淀粉的碘水中发生氧化还原反应,还原剂是二氧化硫、还原产物是碘离子,所以还原性SO2>I-,碘遇淀粉试液变蓝色,所以能表明I-的还原性弱于SO2的现象是:D中蓝色褪去;离子反应方程式为I2+SO2+2H2O=4H++2I-+SO42-。
考点:本题考查实验基本仪器和基本操作、化学实验方案的设计、氧化还原反应原理、离子反应。
本题难度:困难
4、选择题 在化学分析中草酸(H2C2O4)是重要的还原剂,已知20.00?mL?0.100?mol・L-1?VO2+离子恰好将20.00?mL??0.050?mol・L-1?H2C2O4完全氧化成CO2,VO2+被还原为VOn+离子,则VOn+中的n值为
A.1
B.2
C.3
D.4
参考答案:B
本题解析:VO2+与H2C2O4的物质的量比为2:1,即:2VO2+ + 1H2C2O4→2VOn+ + 2CO2,反应中有2个电子的转移,V由+5价降至+4价,得n=2
本题难度:困难
5、选择题 3NO2十H2O====2HNO3十NO为工业上氨催化氧化法制硝酸的反应之一,该反应中NO2的作用是
A.只作氧化剂
B.作催化剂
C.既作氧化剂又作还原剂
D.作还原剂
参考答案:C
本题解析:
试题分析:3NO2十H2O====2HNO3十NO中,N元素的化合价从+4价升高到+5价,被氧化为硝酸,同时N元素的化合价从+4价降低到+2价,被还原为NO,所以二氧化氮既作氧化剂又作还原剂,所以答案选C。
考点:考查氧化剂、还原剂的判断
本题难度:一般