微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 双氧水(H2O2)是一种极弱电解质,也是一种“绿色氧化剂”。为了贮存、运输的方便,工业上将其转化为固态过碳酸钠(2Na2CO4・3H2O),该物质具有Na2CO3与H2O2的双重性质。请回答下列问题:
(1)写出H2O2的电子式:?????????????????????????????????????????????????????????????????????????????????????,并写出它与SO2反应的化学方程式??????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????。
(2)若把H2O2看成二元弱酸,写出它在水中第一步电离的方程式??????????????????????????????????????????????。
(3)下列物质不会使过碳酸钠失效的是?????????????????????????????????????????????????????????????????????????
A.MnO2
B.NaHCO3
C.H2S
D.CH3COOH
(4)稀H2SO4不与Cu反应,但在稀H2SO4中加入H2O2后则可使Cu溶解,写出该反应的化学方程式,并用单线桥标明电子转移的方向和数目。????????????????????????????????????????????????????????????????????????????????????????????????????????????
(5)H2O2成为“绿色氧化剂”的理由是?????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????????。
参考答案:
B
本题解析:略
本题难度:简单
2、填空题 已知A、B、C、D为常见单质,其中B、C、D常温常压下为气体,甲、乙、丙、丁为化合物,乙常温下为液体,丙的焰色反应为黄色,下图为各种物质之间的相互反应
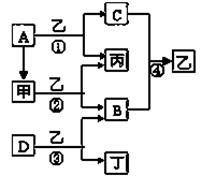
(1)写出下列物质的化学式:
A??????????,B??????????,D??????????,丙?????????。
(2)丙电子式为?????????????,反应②中若有11.2L(标准状况下)B生成,则发生转移的电
子的物质的量为?????????????????????????。
(3)写出反应③的化学方程式:??????????????????????????????????????????????
参考答案:(1)A:钠; B: 氧气;C:氟气;丙:氢氧化钠(2)1
本题解析:
试题分析:丙的焰色反应为黄色且为化合物,故丙为NaOH, 乙常温下为液体,又乙由常见的两种单质气体反应生成,故乙为水,根据A和乙反应生成氢氧化钠和氢气,故C为氢气,B为氧气;单质气体与水反应能生成氧气的是氟气,故D为氟气;甲和水生成氢氧化钠和氧气,则甲为过氧化钠;故(1)A:钠; B: 氧气;C:氟气;丙:氢氧化钠;(2)氢氧化钠的电子式为:Na+ [: O : H]-;②反应为2Na2O2+2H2O===4NaOH+O2。故生成0.5mol的氧气发生转移的电子数为1mol。(3)③的化学反应方程
本题难度:一般
3、选择题 已知:Li与Mg、Be与Al的性质相似。下列判断正确的是
A.LiOH是强碱
B.Be与冷水剧烈反应
C.Li在空气中不易被氧化
D.Be(OH)2能与NaOH溶液反应
参考答案:D
本题解析:
试题分析:A、因为氢氧化镁是中强碱,所以LiOH是中强碱,错误;B、Al与冷水不反应,加热才反应,所以Be与冷水不反应,错误;C、Mg在空气中易生成氧化镁,所以Li在空气中也被氧化为氧化锂,错误;D、氢氧化铝能与氢氧化钠溶液反应,所以Be(OH)2也能与NaOH溶液反应,正确,答案选D。
本题难度:一般
4、选择题 下列关于金属钠及其化合物的叙述正确的是
①烧碱又称纯碱?②钠原子最外层电子只有1个电子,所以在化合物中钠只显+1价?③过氧化钠中阴阳离子个数比为1:1?④钠离子具有还原性,可以从水中还原出氢气?⑤等物质的量的NaHCO3与Na2CO3分别于足量的盐酸反应,产生的CO2量相等,但反应速率前者快。
A.①②③
B.③④⑤
C.②⑤
D.①②⑤
参考答案:C
本题解析:①烧碱为NaOH,而纯碱为Na2CO3;?②正确?③过氧化钠中阴阳离子个数比为2:1?④钠离子具有弱氧化性,可在水中存在,并不与水反应?⑤正确
答案为C
本题难度:简单
5、填空题 (10分)工业碳酸钠(纯度约为98%)中常含有Ca2+、Mg2+、Fe3+、Clˉ和SO42ˉ等杂质,为了提纯工业碳酸钠,并获得试剂级碳酸钠的工艺流程图如下:
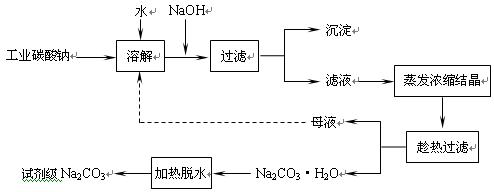
已知:碳酸钠的饱和溶液在不同温度下析出的溶质如下图所示:
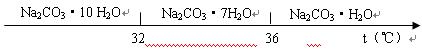
 (1)加入NaOH溶液时发生的离子反应方程式为?? ▲??、?? ▲??。
(1)加入NaOH溶液时发生的离子反应方程式为?? ▲??、?? ▲??。
(2)热的Na2CO3溶液有较强的去油污能力,其原因是(用离子方程式及必要的文字加以解释)?? ▲??。
(3)“趁热过滤”时的温度应控制在?? ▲??。
(4)已知:Na2CO3・10 H2O(s)=Na2CO3(s)+10 H2O(g)??△H=+532.36kJ・mol―1
Na2CO3・10 H2O(s)=Na2CO3・H2O(s)+9 H2O(g)?△H=+473.63kJ・mol―1
写出Na2CO3・H2O脱水反应的热化学方程式?? ▲??。
(5)有人从“绿色化学”角度设想将“母液”沿流程图中虚线所示进行循环使用。请你分析实际生产中是否可行?? ▲??,其理由是?? ▲??。
参考答案:(1)Fe3++3OHˉ=Fe(OH)3↓、MgCO3 +2
本题解析:略
本题难度:一般