微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 判断一个反应是否为氧化还原反应的标准是
A.是否有氧参加反应
B.化合物是否分解
C.同一元素的化合价在反应前后是否发生变化
D.是否为化合或分解反应
参考答案:C
本题解析:
试题分析:氧化还原反应的特征是反应前后同一元素的化合价发生变化,C项正确。
本题难度:简单
2、填空题 从铁、盐酸、氧气、水、碳酸钙五种物质中选出一种或两种作为反应物,按下列要求的反应类型各写一个化学方程式
(1)化合反应______(2)分解反应______(3)置换反应______(4)复分解反应______.
参考答案:因Fe为单质、HCl为化合物、O2为单质,H2O为化合物,C
本题解析:
本题难度:一般
3、选择题 下列有关化学用语使用正确的是
A.乙醇的结构简式:C2H6O
B.NH4Cl的电子式: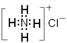
C.原子核内有10个中子的氧原子: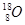
D.次氯酸分子结构式 H―Cl―O
参考答案:C
本题解析:
试题分析:A、C2H6O是乙醇的分子式,错误;B、NH4Cl的电子式中Cl-的电子式不是其简单离子符号,错误;C、O原子核内有8个质子,所以10个中子的氧原子为: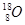 ,正确;D、次氯酸分子结构式H―O―Cl ,错误,答案选C。
,正确;D、次氯酸分子结构式H―O―Cl ,错误,答案选C。
本题难度:简单
4、计算题 (6分)在50mL a mol・L-1的硝酸溶液中,加入6.4g Cu,全部溶解,假设硝酸的还原产物只有NO2和NO,将反应后溶液用蒸馏水稀释至100mL时测得c(NO3-)="3" mol・L-1。
(1)求稀释后的溶液的pH= 。
(2)若a=9,则生成的气体中NO2的物质的量为 mol。
(3)治理氮氧化物污染的方法之一是用NaOH溶液进行吸收,反应原理如下:
NO2+NO+2NaOH=2NaNO2+H2O 2NO2+2NaOH=NaNO2+NaNO3+H2O
若将上述的NO2和NO的混合气体通入1mol・L-1的NaOH恰好被吸收,求NaOH溶液的体积为 mL。
参考答案:(6分)(1)0 (2)0
本题解析:
试题分析:(1)Cu的物质的量是0.1mol,反应后的溶液中NO3-的物质的量是0.3mol,说明反应后的溶液为硝酸铜与硝酸的混合液,根据电荷守恒,其中氢离子的物质的量是0.1mol,浓度是1mol/L,所以稀释后溶液的pH=0;
(2)若a=9,则原硝酸溶液中硝酸的物质的量是0.45mol,根据(1)可知反应后溶液中NO3-的物质的量是0.3mol,所以被还原的硝酸的物质的量是0.15mol,设混合气体中NO2的物质的量为xmol,NO的物质的量是ymol,则x+y=0.15,x+3y=0.1×2,解得x=0.125mol,y=0.025mol;
(3)根据(2)的结果,结合化学方程式计算需要氢氧化钠的物质的量是0.15mol,所以1mol・L-1的NaOH溶液的体积是150mL。
考点:考查氧化还原反应的计算
本题难度:一般
5、选择题 下列有关化学用语以及化学基本概念的表述中正确的一组是( )
A.过氧乙酸(CH3COOOH)与羟基乙酸(HOCH2COOH)所含官能团相同,两者互为同分异构体
B.日本福岛核电站泄露的放射性核素Ⅰ和Cs,前者比后者少4个中子
C.亚硫酸氢钠和碳酸氢钠的电离方程式都表示为NaHRO3?Na++HRO(R=C或S)
D.次氯酸的结构式为HOCl,过氧化氢的电子式为H+[O O]2-H+
参考答案:B
本题解析:A错,过氧乙酸(CH3COOOH)与羟基乙酸(HOCH2COOH)所含官能团不相同;
B正确,Ⅰ的中子数=131―53=78;Cs的中子数=137―55=82,两者中子数之差为4;
C错,亚硫酸氢钠和碳酸氢钠均为强电解质,电离方程式不能用可逆符号;
D错,次氯酸的结构式为H―O―Cl,过氧化氢的电子式为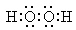 本题难度:一般
本题难度:一般