��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����Ȼ�ѧ����ʽ�У���H����ȷ��ʾ���ʵ�ȼ���ȵ���(����)
A��S(s)��O2(g)===SO2(g)����H����269.8 kJ/mol
B��C(s)��1/2O2(g)===CO(g)����H����110.5 kJ/mol
C��H2(g)��1/2O2(g)===H2O(g)����H����241.8 kJ/mol
D��2C8H18(l)��25O2(g)===16CO2(g)��18H2O(l)��H����11036 kJ/mol
�ο��𰸣�A
���������ȼ��������һ�������£�1mol��ȼ����ȫȼ�������ȶ���������ʱ���ų�������������ѡ��A��ȷ��B��̼û����ȫȼ�գ�C��ˮ���ȶ�״̬Ӧ����Һ̬��D�п�ȼ�ﲻ��1mol�����Ǵ���ģ����Դ�ѡA��
�����Ѷȣ�һ��
2��ѡ���� ���е������Ba��OH��2��NaOH��NH3��H2O������Һ�������Ƿֱ���V1L��V2L��V3L��Ũ�ȵ������ϣ�����˵������ȷ����??????????????????��???��
A�������ǰ����ҺpH��ȣ�������ͬ�ȱ���ϡ�ͺ�NaOH��ҺpH���
B�������ǰ����ҺpH��ȣ����ǡ����ȫ��Ӧ����V1>V2>V3
C�������ǰ����Һ���ʵ���Ũ����ȣ����ǡ����ȫ��Ӧ����V1>V2>V3
D�������ǰ����Һ���ʵ���Ũ����ȡ���Ϻ���Һ�����ԣ���V1>V2>V3
�ο��𰸣�D
���������
A������ȷ��Ba(OH)2��ҺpH���;
B������ȷ�� V1=V2???<V3
C������ȷ��V1=V2=V3
D����ȷ��ѡD��
�����Ѷȣ�һ��
3������� (8��)��ѧ������̫���ֽܷ�ˮ���ɵ������ڴ����������������̼��Ӧ���ɼ״�����������ֱ���Լ״�Ϊȼ�ϵ�ȼ�ϵ�ء���ش��������⣺
��1����֪�� ��CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ��H=+49.0kJ/mol
��CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) ��H=��192.9kJ/mol
����������ʽ��֪��CH3OH(g)��ȼ����____������ڡ��������ڡ���С�ڡ���192.9kJ/mol����֪ˮ��������Ϊ44 kJ/mol�����ʾ����ȼ���ȵ��Ȼ�ѧ����ʽΪ______________________________��
��2�����ݻ�Ϊ2 L���ܱ������У���CO2��H2�ϳɼ״����������������������£������¶ȶԷ�Ӧ��Ӱ�죬ʵ��������ͼ��ʾ��ע��T1��T2������300 �棩
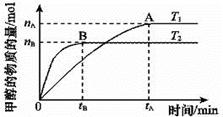
�÷�ӦΪ_________��Ӧ(����ȡ������ȡ�)����T1�¶�ʱ����1 mol CO2��3 mol H2����һ�ܱպ������У���ַ�Ӧ�ﵽƽ�����CO2ת����Ϊa���������ڵ�ѹǿ����ʼѹǿ֮��Ϊ____________________��
�ο��𰸣���1������H2 (g)+1/2O2 (g)=H2O(l)&#
���������
�����������1���״���ȼ������1mol�ļ״���ȫȼ�ղ����ȶ���������ʱ���ų���������ˮ�������µ��ȶ�״̬��Һ�壬1mol�ļ״��״���ȫȼ�ղ�����̬ˮʱ���ų���������192.9kJ,����ˮ������ΪҺ̬ˮʱ��ų�����������ȼ����Ҫ����192.9kJ/mol�����ڣ��٣���3�ɵ�H2 (g)+1/2O2 (g)=H2O(g) ��H=��80.6KJ/mol������ˮ��������Ϊ44 kJ/mol�����ʾ����ȼ���ȵ��Ȼ�ѧ����ʽΪH2 (g)+1/2O2 (g)=H2O(g) ��H=��124.6KJ/mol����2�����������¶ȣ��״���ƽ�⺬�����٣�����ƽ���ƶ�ԭ���������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ����淴ӦΪ���ȷ�Ӧ��˵���ϳɼ״��ķ�Ӧ���ȷ�Ӧ���ں���ʱ����������ʵ����ıȵ���ѹǿ֮�ȣ�CO2(g)+3H2(g)=CH3OH(g)+H2O(g)�����ڼ�����1mol��CO2��������ת����Ϊa����ﵽƽ��ʱ�������ʵ����ʵ�����CO2 :(1-a)mol; H2��3(1-a)mol; CH3OH��amol��H2O��amol��n(ƽ��)��n(��ʼ)= [(1-a)��3(1-a)��a��a]����1+3)=(4-2a��:4= (2-a):2��
���㣺�����Ȼ�ѧ����ʽ����д��ȼ���ȡ���Ӧ�ȵ��жϼ��� ѹʱ�����ѹǿ�ȵĹ�ϵ��֪ʶ��
�����Ѷȣ�һ��
4��ѡ���� ij��Ԫ�ᣨH2A������ʽ�������룺H2A��H++HA����HA�� H++A2������������������Һ��
H++A2������������������Һ��
�� 0.01mol?L1��H2A��Һ
�� 0.01mol?L1��NaHA��Һ
�� 0.02mol?L1��HCl��Һ��0.04mol?L1��NaHA��Һ��������
�� 0.02mol?L1��NaOH��Һ��0.02mol?L1��NaHA��Һ��������
���й�������������Һ��˵����ȷ���ǣ�???��
A����Һ���д���ˮ��ƽ�⣺HA�D+H2O 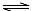 H2A+OH�D
H2A+OH�D
B����Һ�����У�c(HA��)+2c(A2��)=c(Na+)
C����Һ�����У�c(OH��)=c(H+)+c(HA��)
D��������Һ��c (HA��)Ũ�ȴ�С���ۣ��٣��ڣ���
�ο��𰸣�CD
���������
�����������Ԫ��H2A��ˮ��Һ�з������룺H2A��H++HA-��HA- H++A2-����˵���Ƕ�Ԫ��ĵ�һ����������ȫ�ģ����ڶ���������ڵ���ƽ�⡣���HA-����ֻ���ڵ���ƽ�⣬������ˮ��ƽ�⣬��Һ�����ԣ�ѡ��A����ȷ��B����ȷ�������������غ㣬Ӧ����c(HA��)+c(A2��)=c(Na+)������ǡ�÷�Ӧ
H++A2-����˵���Ƕ�Ԫ��ĵ�һ����������ȫ�ģ����ڶ���������ڵ���ƽ�⡣���HA-����ֻ���ڵ���ƽ�⣬������ˮ��ƽ�⣬��Һ�����ԣ�ѡ��A����ȷ��B����ȷ�������������غ㣬Ӧ����c(HA��)+c(A2��)=c(Na+)������ǡ�÷�Ӧ
�����Ѷȣ�����
5��ѡ���� ����Һ��pH=6������Һ��pH=2��������������ȷ����(??? )
A���ס�������Һ��c(H+)֮��Ϊ400��1
B������ˮ�ĵ���̶�������ˮ�ĵ���̶����Ƚ�
C������ˮ�ĵ���̶�С������ˮ�ĵ���̶�
D���ס�������Һ��������
�ο��𰸣�B
�����������
�����Ѷȣ�һ��