微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、推断题 今有原子序数依次增大的A、B、C、D、E、F六种元素。已知A、C、F三原子的最外层共有11 个电子,这三种元素的最高价氧化物的水化物之间两两皆能反应且均生成盐和水。D和E各有如 下表所示的电子层结构。在一般情况下,B元素的单质不能与A、C、D、E元素的单质化合。

按要求填空:
(1)各元素的元素符号分别为C____。E__,D和E两者的氢化物稳定性较强的是___(填化学式)。
(2)工业上制取单质D的化学方程式为___。
(3)A与C两元素的最高价氧化物对应的水化物反应的离子方程式为___。
(4)E与F形成E的最高价化合物,0.25 mol该固体物质与足量水充分反应,最终生成两种酸,并放出akJ的热量。写出该反应的热化学方程式:___。
参考答案:(1)Al; P ;PH3
(2) SiO2+2C<
本题解析:
本题难度:一般
2、选择题 第三周期元素R,它的原子最外电子层上达到饱和所需电子数小于次外层和最内层电子数之差,但等于最内层电子数的正整数倍。下列说法正确的是 [???? ]
A.常温下,能稳定存在的R的氧化物都能与烧碱溶液反应
B.R的最高价氧化物对应的水化物都是强酸
C.在固态时,R的单质都属于熔点很高的非金属
D.在常温下,R的气态氢化物都能在空气中稳定存在
参考答案:A
本题解析:
本题难度:一般
3、推断题 X、Y、Z、L、M五种元素的原子序数依次增大.X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素.回答下列问题:
(1)L的元素符号为________;M在元素周期表中的位置为________;五种元素的原子半径从大到小的顺序是__________________(用元素符号表示).
(2)Z、X两元素按原子数目比1∶3和2∶4构成分子A和B,A的电子式为________,B的结构式为________.
(3)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为________,其最高价氧化物对应的水化物化学式为________,该族2~5周期元素单质分别与H2反应生成1?mol气态氢化物的反应热如下,表示生成1?mol硒化氢反应热的是________(填字母代号).
a.+99.7?kJ/mol b.+29.7?kJ/mol ?c.-20.6?kJ/mol?? d.-241.8?kJ/mol
参考答案:(1)O;第3周期第ⅢA族;Al>C>N>O>H
(2
本题解析:
本题难度:一般
4、简答题 右图是元素周期表的一部分,各元素在周期表中的位置如下,据此回答下列问题:
| a | |
e
g
i
j
b
c
d
f
h
k
l
(1)下列各组元素中最容易形成离子键的是______,最容易形成共价键的是______
A、c和h?????B、b和k????C、e和j??????D、e和i
(2)下列由a~k形成的各分子中,所有原子都满足最外层电子数8电子结构的是______
A、ga3?????B、ak???C、hk3???D、ek4
(3)请用化学方程式解释下列现象
①玻璃容器不能盛放j的氢化物的水溶液:______
②b的氧化物对应的水化物溶液不能贮存在d制品中:______.
参考答案:根据元素周期表的结构和元素的分布知识,可知a是H,b是Na,
本题解析:
本题难度:一般
5、选择题 甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:甲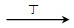 乙 乙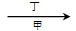 丙。下列有关物质的推断不正确的是??????????????????? ( )。 丙。下列有关物质的推断不正确的是??????????????????? ( )。
A.若甲为焦炭,则丁可能是O2
B.若甲为SO2,则丁可能是氨水
C.若甲为Fe,则丁可能是盐酸
D.若甲为NaOH溶液,则丁可能是CO2
参考答案:C
本题解析:若甲为焦炭,丁为O2,转化关系为:C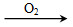 CO CO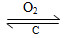 CO2,A正确;若甲为SO2,丁为氨水,转化关系为:SO2 CO2,A正确;若甲为SO2,丁为氨水,转化关系为:SO2![]()
本题难度:一般
|