微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 二氧化氯(ClO2)作为一种高效强氧化剂,已被联合国世界卫生组织(WHO)列为AI级安全消毒剂。常温下二氧化氯为黄绿色或橘黄色气体,性质非常不稳定。温度过高,二氧化氯的水溶液有可能爆炸。某研究小组设计如图所示实验制备ClO2。
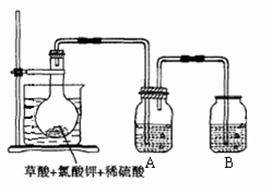
(1)如图,在烧瓶中先放入一定量的KClO3和草酸(H2C2O4),然后再加入足量的稀硫酸,水浴加热。反应后产物中有ClO2、CO2和一种酸式盐,该反应的化学方程式为:??????????????????,氧化产物与还原产物的物质的量之比为 ??????????????。
(2)控制水浴温度在60~80℃之间的目的是???????????????????????????????,图示装置中缺少的一种必须的玻璃仪器是???????????????????????????????。
(3)A装置用于吸收产生的二氧化氯,其中最好盛放????????????。(填序号)
①60 ℃的温水? ②冰水??? ③饱和食盐水??
(4)将二氧化氯溶液加入到硫化氢溶液中,所得溶液中加入少量氯化钡溶液,有白色沉淀生成。请写出二氧化氯溶液和硫化氢溶液反应的化学方程式???????????????。
参考答案:(1)2KClO3+H2C2O4+2H2SO4![]()
本题解析:
试题分析:(1)根据提示可知反应的方程式为2KClO3+H2C2O4+2H2SO4 2ClO2↑+2CO2↑+2KHSO4+2H2O。氧化产物和还原产物的物质的量之比为1:1。
2ClO2↑+2CO2↑+2KHSO4+2H2O。氧化产物和还原产物的物质的量之比为1:1。
(2)如果温度过高,会引起爆炸,缺少的必要玻璃仪器是温度计。
(3)因为二氧化氯水溶液温度过高会引起爆炸,所以应该用冰水来吸收。
(4)根据提示可知该反应的方程式为:5H2S+8ClO2+4H2O=5SO42-+8Cl-+18H+。
点评:本题主要考查学生获得信息的能力和实验分析能力。
本题难度:一般
2、填空题 (10分)化学实验室通常用粗锌和稀硫酸反应制氢气,因此在制氢废液中含有大量的硫酸锌。同时,由于粗锌中还含有铁等杂质,使得溶液中混有一定量的硫酸亚铁,为了充分利用制氢废液,常用其制备皓矾(ZnSO4・7H2O)。某校化学兴趣小组的同学以制氢气的废液为原料来制取皓矾。制备皓矾的实验流程如下图所示。
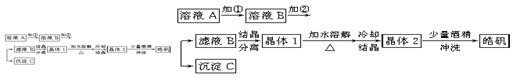
已知:开始生成氢氧化物沉淀到沉淀完全的pH范围分别为:Fe(OH)3:2.7-3.7
Fe(OH)2:7.6-9.6? Zn(OH)2:5.7-8.0试回答下列问题:?
(1)加入的试剂①,供选择使用的有:氨水、NaClO溶液、20%的H2O2、浓硫酸、浓硝酸等,最好选用????????,其理由是???????????????????????????????????????;
(2)加入的试剂②,供选择使用的有:a、Zn粉,b、ZnO,c、Zn(OH)2,d、ZnCO3,e、ZnSO4等,可选用?????????????;
(3)从晶体1→晶体2,该过程的名称是???????;
(4)在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是???????????????。
参考答案:
(1)20%的H2O2(2分)???将制氢废液中的F
本题解析:
试题分析:
(1)本题需要把Fe3+转化为Fe2+,使用的试剂有氧化性,并且不能引入新的杂质,使用20%的H2O2是最佳的选择。
(2)能调节溶液pH值,而不引入新的杂质。
(3)重结晶的作用是使结晶更加纯净。
(4)不能用水,否则晶体会重新溶解。用酒精洗涤掉晶体表面的杂质离子。
点评:本题以工业制皓矾为背景,结合生产实际。试题过程解答不难,需要抓住题目的关键,熟悉各个实验步骤的用途。
本题难度:困难
3、选择题 利用下列各组中的物质制备并收集相应的气体,能采用如图所示装置的是

A.浓氨水和固体NaOH制NH3
B.过氧化氢溶液和二氧化锰制O2
C.稀硝酸和铜片制NO
D.电石和饱和食盐水制乙炔
参考答案:B
本题解析:A中虽能制取氨气,但不能用此方法收集氨气,因为它的密度比空气小;C中NO能被空气中氧气氧化,不能用排空气法收集。D中乙炔也不能向上排空气法收集。答案选B。
本题难度:一般
4、实验题 (11分)某同学按下列步骤配制500 mL 0.2 mol・L-1 KCl溶液,请回答下列问题:
实验步骤
| 有关问题
|
(1)计算所需KCl的质量
| 需要KCl的质量为______g
|
(2)称量KCl固体
| 称量过程中主要用到的仪器有________________
|
(3)将KCl放入到100 mL烧杯中加水溶解
| 为加快溶解速度,可采取的措施是______________________
|
(4)将烧杯中的溶液转移至500 mL容量瓶中
| 为防止溶液溅出,应采取的措施是____________________
|
(5)向容量瓶中加蒸馏水到刻度线
| 在进行此操作时应注意的问题是__________________________
你认为按上述步骤配制的KCl溶液的浓度是否为0.2 mol・L-1,请说明理由。
参考答案:
实验步骤
有关问题
(1)
本题解析:根据配制一定物质的量浓度溶液的步骤:
(1)n(KCl)=0.5 L×0.2 mol・L-1=0.1 mol
m(KCl)=74.5 g・mol-1×0.1 mol=7.45 g
(2)称KCl固体质量,所用仪器:天平、药匙。
(3)为加快溶解,可称前研细,溶解时搅拌或加热。
(4)为了防止移液时液体溅出,可采用玻璃棒引流。
(5)加蒸馏水时,用玻璃棒引流,加入蒸馏水至离刻度线1~2 cm处,改用胶头滴管滴加至刻度线。由于移液时未洗涤烧杯和玻璃棒,配制溶液的浓度低于0.2 mol・L-1。
本题难度:一般
5、实验题 下图所示为常见气体制备、分离、干燥和性质验证的部分仪器装置(加热设备及夹持固定装置均略去),请根据要求完成下列各题(仪器装置可任意选用,必要时可重复选择,a、b为活塞)。
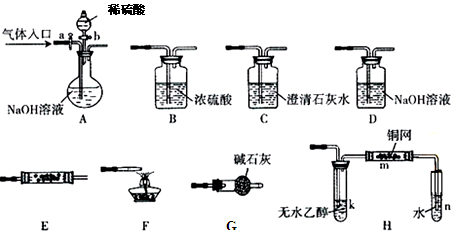
(1)若气体入口通入CO和CO2的混合气体,E内放置CuO,选择装置获得纯净干燥的CO,并验证其还原性及氧化产物,所选装置的连接顺序为 (填代号)。能验证CO氧化产物的现象是 。
(2)停止CO和CO2混合气体的通入,E内放置Na2O2,按A→E→D→B→H装置顺序制取纯净干燥的O2,并用O2氧化乙醇。此时,活塞a应 ,活塞b应 ,需要加热的仪器装置有 (填代号),m中反应的化学方程式为: 。
(3)若气体入口改通空气,分液漏斗内改加浓氨水,圆底烧瓶内改加NaOH固体,E内放置铂铑合金网,按A→G→E→D装置顺序制取干燥的氨气,并验证氨的某些性质。
①装置A中能产生氨气的原因有 。
②实验中观察到E内有红棕色气体出现,证明氨气具有 性。
参考答案:(1)ACBECF(2分)?? AB之间的C装置中溶液保持澄
本题解析:
试题分析:(1)用A装置的NaOH来除CO中混有的CO2,(生成Na2CO3),用C装置检验有没有除尽CO2,B装置是干燥气体的,纯净的CO,通入E中,生成的CO2能使装置C有沉淀,多余的CO在装置F处尾气吸收。
(2)关闭装置A的活塞a,停止通入CO和CO2,打开活塞b,使稀硫酸和A中的碳酸钠反应,产生CO2,通入E,和Na2O2,产生O2,用D吸收O2混有的CO2,用B干燥O2中的H2O,纯净的O2在H中和乙醇发生催化氧化反应。加热k产生乙醇蒸汽,加热m ,是因为乙醇催化氧化需要催化剂铜和加热条件。
(3)这过程发生的反应为4NH3+5O2=4NO+6H2O(NH3表现还原性);2NO+O2=2NO2(红棕色)。
本题难度:一般
|