微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
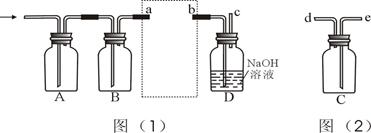
1、实验题 (10分)实验室制得的氯气通常含有水蒸气和盐酸挥发的氯化氢,要制取干燥纯净的氯气,可用如图所示的装置,进行干燥、净化、收集和尾气处理(C瓶用于收集氯气,D瓶用于尾气处理)。
据此完成下列各题:
(1)实验室通常用饱和食盐水吸收杂质HCl,则图(1)中A瓶和B瓶依次分别盛装的试剂是:_____________________________________;
(2)图(2)是氯气的收集装置,将它安置在图(1)中的虚线框内,其导管的连接顺序是:______________________________;
(3)检查最终尾气排放(导管口c处)是否含有氯气,可用湿润的淀粉-KI试纸测试,如有氯气泄漏,可观察到__________________________________,产生此现象的直接原因是__________________________________;此方法检测氯气,试纸必须用水润湿是因为________________________________________。
参考答案:(10分,每空2分)(1)饱和食盐水、浓硫酸;(2)a连e,
本题解析:略
本题难度:简单
2、填空题 (7分)⑴用18mol/L浓硫酸配制100mL 1.0mol/L的稀硫酸,若实验仪器有:
A.100mL量筒? B.玻璃棒 ?? C.托盘天平 D.50mL容量瓶
E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
实验时必须选用的仪器是(填入字母)???????????????
?
?
⑵在配制过程中,下列操作不正确的是??????????????????A.使用容量瓶前需检查它是否漏水
B.容量瓶用蒸馏水洗净后,一定要干燥后再使用
C.配制溶液时,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水至刻度线
D.定容后盖好瓶塞,反复上下颠倒,摇匀
⑶若实验时遇到下列情况,将使所配溶液的浓度????????(填“偏高”、“偏低”或“无影响”)
A.定容时俯视读数????????????B.未将洗涤液转入容量瓶?????????
C.洗涤量筒,并将洗涤液转入容量瓶????????
参考答案:(7分)(1)BEFGH(2分)??(2)BC (2分)
本题解析:(1)所需浓硫酸的体积为18×V=0.1×1,得V=0.0056L=5.6ml,故需要用到10mL量筒、玻璃棒、烧杯、胶头滴管、100mL容量瓶
(2)A:正确
B:容量瓶没有必要干燥
C:硫酸必须在烧杯中溶解稀释冷却后再移液至容量瓶
D:正确
(3)A:加水偏少,所配溶液浓度偏高
B:未将洗涤液转入容量瓶,导致部分溶质未转移至容量瓶中,浓度偏低
C:量筒不必洗涤,否则溶质偏多,溶液浓度偏高
本题难度:简单
3、实验题 NiSO4?6H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有:Cu、Zn、Fe、Cr等元素的化合物杂质)为原料获得。有关工艺流程如下:
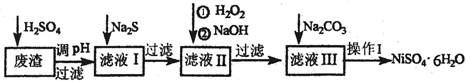
(1)往废渣中加H2SO4酸漫,要充分搅拌,其目的是???????????????????。
(2)加Na2S的目的是除去铜、锌等杂质,请写出除去Cu2+的离子方程式????????????。
(3)加6%的H2O2时,温度不能过高,其目的是????????????????????????。
(4)除铁方法:用H2O2充分氧化后,再用NaOH控制pH值2~4范围内生成氢氧化铁沉淀。在上述方法中,氧化剂可用NaClO3代替,用NaClO3氧化Fe2+的离子方程式为???????????????????????????????????????。
(5)上述流程中滤液III的溶质的主要成分是:???????????????????。
(6)操作I包括以下过程:过滤,用H2SO4溶解,???????????????、??????????????、过滤、洗涤获得产品。
参考答案:(16分)(1)加快反应速率或提高浸出率(合理的给分)?(2
本题解析:
试题分析:(1)根据化学反应速率的影响因素及规律可知,充分搅拌的目的是加快废渣中的镍单质等与硫酸反应的速率,提高镍元素的浸出率;(2)Na2S是可溶性盐,溶于水时电离出S2ˉ,S2ˉ与Cu2+易反应生成CuS沉淀;(3)过氧化氢是绿色氧化剂,其目的是将Fe2+完全氧化为Fe3+,且不引入新的杂质,但是H2O2不稳定,受热易分解为水和氧气,因此温度不能过高;(4)NaClO3是可溶性盐,NaOH是强碱,根据题意可知,Fe2+是还原剂,ClO3ˉ是氧化剂,Fe3+是氧化产物,还原产物是Clˉ,而不是Cl2,因为碱性溶液不能大量存在Cl2,根据铁元素化合价升高总数等于氯元素化合价降低总数,电荷守恒、原子守恒原理可得反应式:6Fe2++ClO3ˉ+6H+=6Fe3++Clˉ+3H2O;(5)读图可知,加Na2S的目的是除去铜、锌等杂质,加H2O2、NaOH的目的是除去铁等杂质,加Na2CO3的目的是除去铬等杂质,因此推断滤液1的主要成分是NiSO4、FeSO4、Cr2(SO4)3、Na2SO4,滤液II的主要成分是NiSO4、Cr2(SO4)3、Na2SO4,滤液III的主要成分是NiSO4、Na2SO4;(6)从NiSO4、Na2SO4及硫酸的混合溶液中制取NiSO4?6H2O晶体,需要蒸发浓缩、冷却结晶、过滤、洗涤、干燥等过程。
本题难度:一般
4、实验题 已知乙醇可以和氯化钙反应生成微溶于水的CaCl2・6C2H5OH。有关的有机试剂的沸点如下:CH3COOC2H5为77.1℃;C2H5OH为78.3℃;C2H5OC2H5(乙醚)为34.5℃;CH3COOH为118℃。实验室合成乙酸乙酯粗产品的步骤如下:在蒸馏烧瓶内将过量的乙醇与少量浓硫酸混合,然后经分液漏斗边滴加醋酸,边加热蒸馏。由上面的实验可得到含有乙醇、乙醚、醋酸和水的乙酸乙酯粗产品。
(1)反应中加入的乙醇是过量的,其目的是????????????????????????????????????。
(2)边滴加醋酸,边加热蒸馏的目的是??????????????????????。
将粗产品再经下列步骤精制:
(3)为除去其中的醋酸,可向产品中加入?????????(填字母)。
A.无水乙醇??????? B.碳酸钠粉末??????? C.无水醋酸钠
(4)再向其中加入饱和氯化钙溶液,振荡,分离,其目的是???????????????????。
(5)然后再向其中加入无水硫酸铜,振荡,其目的是??????????????????。最后,将经过上述处理后的液体加入另一干燥的蒸馏瓶内,再蒸馏,弃去低沸点馏分,收集沸点在76℃~78℃之间的馏分即得纯净的乙酸乙酯。
参考答案:(1)增大反应物乙醇的浓度,有利于反应向生成乙酸乙酯的方向进
本题解析:
试题分析:(1)制取乙酸乙酯的反应是可逆反应,增大反应物乙醇的浓度,有利于反应向生成乙酸乙酯的方向进行;
(2)乙酸乙酯、乙醇、乙醚的沸点较低,边加醋酸边蒸馏,目的使产品蒸出,减小乙酸乙酯的浓度,同时增大醋酸的浓度,使平衡正向进行;
(3)乙酸乙酯不溶于水,醋酸与碳酸钠反应生成醋酸钠、水、二氧化碳气体,所以溶于水的物质在下层,不溶于水的乙酸乙酯在上层,分液可使混合物分离,因此除去产品中的醋酸,应选择碳酸钠溶液,答案选B;
(4)粗产品中仍含有乙醇、乙醚、水,其中乙醇可以和氯化钙反应生成微溶于水的CaCl2・6C2H5OH,所以加入饱和的氯化钙溶液,目的是除去粗产品中的乙醇;
(5)无水硫酸铜与水结合生成蓝色的CuSO4・5H2O,所以加入无水硫酸铜,振荡,其目的是除去粗产品中的水,然后蒸馏可得乙酸乙酯。
本题难度:一般
5、选择题 如图装置可用于收集气体并验证其化学性质,下列对应关系完全正确的是( )
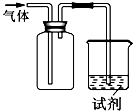
A.气体NO,试剂紫色石蕊试液,现象溶液变红,结论NO与水反应生成硝酸
B.气体Cl2,试剂KI淀粉溶液,现象溶液变蓝,结论Cl2有氧化性
C.气体SO2,试剂酸性KMnO4溶液,现象溶液褪色,结论SO2有漂白性
D.气体NH3,试剂酚酞试剂,现象溶液变红,结论NH3有碱性
参考答案:A、NO易与氧气反应,不能用排空法收集,故A错误;
B
本题解析:
本题难度:简单
|