微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 钢铁工业对促进经济和社会发展起了重要作用。
(1)炼铁高炉分为五部分,铁矿石与高温煤气主要在________部分发生反应,在________部分开始生成生铁和炉渣。
(2)炼钢时,除磷的化学方程式为____________________;加入硅、锰和铝的目的是________________________。
(3)不锈钢含有的Cr元素是在炼钢过程的氧吹________(填“前”或“后”)加入,原因是______________________。
(4)炼铁和炼钢生产中,尾气中均含有的主要污染物是________。从环保和经济角度考虑,上述尾气经处理可用作________。
参考答案:(1)炉身 炉腰
(2)2P+5FeO+3CaO
本题解析:(2)炼钢时,P被FeO氧化,生成的P2O5与CaO结合成Ca3(PO4)2而除去,据此即可写出方程式。
(4)炼铁尾气主要含有N2、CO、CO2等,炼钢尾气主要含有CO、CO2、Fe2O3粉尘等,共同的主要污染物为CO。
本题难度:一般
2、填空题 海洋是一个丰富的资源宝库,通过海水的综合利用可获得许多物质供人类使用。
(1)海水中盐的开发利用:
①海水制盐目前以盐田法为主,建盐田必须选在远离江河人海口,多风少雨,潮汐落差大且又平坦空旷的海滩。所建盐田分为贮水池、蒸发池和??????池。
②目前工业上采用比较先进的离子交换膜电解槽法进行氯碱工业生产,在电解槽中阳离子交换膜只允许阳离子通过,阻止阴离子和气体通过,请说明氯碱生产中阳离子交换膜的作用:
?????????????????????????????????????????????????????(写一点即可)。
(2)电渗析法是近年来发展起来的一种较好的海水淡化技术,其原理如图所示。其中具有选择性的阴离子交换膜和阳离子交换膜相间排列。请回答下面的问题:
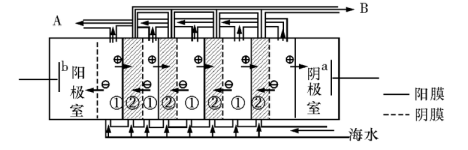
①海水不能直接通人到阴极室中,理由是???????????????????。
②A口排出的是?????????(填“淡水”或“浓水”)。
(3)用苦卤(含Na+、K+、Mg2+、Cl-、Br-等离子)可提取溴,其生产流程如下:
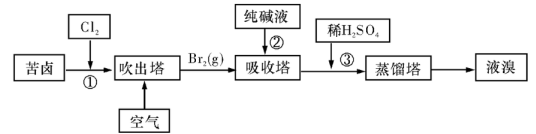
①若吸收塔中的溶液含Br03-,则吸收塔中反应的离子方程式为:??????????????????。
②通过①氯化已获得含Br2的溶液,为何还需经过吹出、吸收、酸化来重新获得含Br2的溶液?
③向蒸馏塔中通入水蒸气加热,控制温度在90℃左右进行蒸馏的原因是
参考答案:(1)①结晶②阻止氢气与氯气发生反应甚至发生爆炸或阻止氯气与
本题解析:
试题分析:(1)①海水制盐中的盐田法中所建盐田分为贮水池、蒸发池和结晶池;
②电解槽中阳离子交换膜只允许阳离子通过,阻止阴离子和气体通过,避免了氢气和氯气接触而发生反应甚至爆炸,同时也避免了氯气与生成的氢氧化钠溶液反应而使烧碱产品不纯;
(2)①、海水中含有较多的Ca2+和Mg2+等阳离子,电解时阴极附近氢氧根离子浓度增大,与海水中的Ca2+和Mg2+等阳离子结合会产生Mg(OH)2、Ca(OH)2等沉淀从而堵塞阳离子交换膜,所以海水不能直接通人到阴极室中;
②、A口排出的是图中
本题难度:一般
3、选择题 海水资源的综合利用十分重要,不需要通过化学变化就能够从海水中获得的物质是
A.食盐、淡水
B.钠、镁
C.烧碱、氯气
D.溴、碘
参考答案:A
本题解析:
试题分析:A、将海水蒸发即可得到食盐,正确;B、需要用电解的方法,错误;C、需要氯碱工业得到相关产品,错误;D、需要置换反应得到,错误。
本题难度:简单
4、填空题 煤是重要的能源,也是生产化工产品的重要原料。试用所学知识,解答下列问题:
(1)煤的转化技术包括煤的气化技术和液化技术。煤的液化技术又分为???和????。
(2)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理如下图所示:
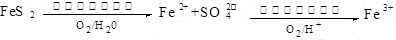 ?
?
这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为??????????????????????,第二步反应的离子方程式为??????????????????????。
(3)工业煤干馏得到的产品有焦炭、??????。
(4)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨―空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上γ{n(O2)/n(NH3)}=?????????,实际生产要将γ值维护在1.7―2.2之间, 原因是????????。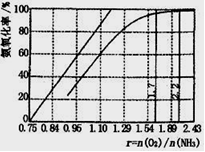
参考答案:(共8分)(1)直接液化技术、间接液化技术(全对给1分)
本题解析:
试题分析:(1)煤的液化分为直接液化和间接液化技术。
(2)第一步反应中反应物有FeS2、O2和H2O,生成物有Fe2+和SO42-,反应中S元素的化合价从-1价升高到+6价,失去7个电子。氧元素的化合价从0价降低到-2价,所以根据化合价升降总数相等以及原子守恒可知,该反应的离子方程式为2FeS2+7O2+2H2O 本题难度:一般
本题难度:一般
5、选择题 综合利用海水可以为人类提供丰富的化学资源,下述说法不正确的是
A.可以从海水中制取Br2
B.可以从海水中制取金属Mg
C.可以从海水中直接提取NaCl
D.可以从海水中直接提取金属Na
参考答案:D
本题解析:A的原理是将海水中的Br-氧化成Br2;
B的原理是先将海水中的Mg2+转化成Mg(OH)2沉淀,再转化成MgCl2,经干燥后电解熔融的MgCl2得金属单质Mg;
在海水中存在的是Na+,故不可直接提取金属单质Na,D错误;
本题难度:简单