微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 用图所示的装置进行电解。通电一会儿,发现湿润的淀粉KI试纸的C端变为蓝色。
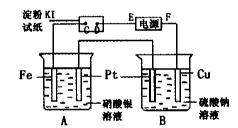
(1)A中发生反应的化学方程式为????????。
(2)在B中观察到的现象是??????????。
(3)室温下,若从电解开始到结束,A、B装置中共收集到气体0.168 L(标况),若电解过程中无其他副反应发生,经测定电解后A中溶液体积恰为1000mL,求A溶液的pH。
参考答案:
 本题解析:略
本题解析:略
本题难度:一般
2、实验题 盐酸、硫酸和硝酸是中学阶段常见的“三大酸”,请就“三大酸”的性质,回答下列问题:
⑴稀盐酸与铜不反应,但向稀盐酸中加入H2O2后,则可使铜溶解。该反应的化学方程式为________________________________________________________。
某同学未加入氧化剂,而是 设计了一个实验装置,也能使铜很快溶于稀盐酸.请在下面的方框中画出该装置:
设计了一个实验装置,也能使铜很快溶于稀盐酸.请在下面的方框中画出该装置:

⑵某课外活动小组设计了以下实验方案验证Cu与浓硝酸反应的过程中可能产生NO。其实验流程图如下:
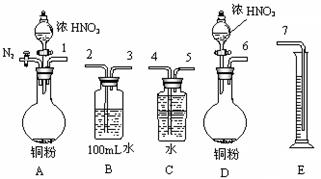
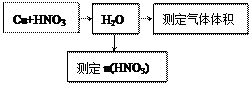
①若要测定NO的体积,从上图所示的装置中,你认为应选用???????装置进行Cu与浓硝酸反应实验,选用的理由是????????????????????????????????????。
②选用如上图所示仪器组合一套可用来测定生成NO体积的装置,其合理的连 接顺序是
??????????????????(填各导管口编号)。
③在测定NO的体积时,若量筒中水的液面比集气瓶的液面要低,此时应将量筒的位置_______(“下降”或“升高”),以保证量筒中的液面与集气瓶中的液面持平。
⑶工业制硫酸时,硫铁矿(FeS2)高温下空气氧化产生二氧化硫:4FeS2+11O2→8SO2+2Fe2O3,设空气中N2、O2的含量分别为0.800和0.200(体积分数),4.8t FeS2完全制成硫酸,需要空气的体积(标准状况)为???????L。
参考答案:
 本题解析:略 本题解析:略
本题难度:一般
3、选择题 近年来,加“碘”食盐较多使用了碘酸钾,KIO3在工业上可用电解法制取,以石墨和铁为电极,以KI溶液为电解液在一定条件下电解,反应式为KI+H2O→KIO3+H2↑(未配平)。下列有关说法中,正确的是[???? ]
A.电解时,石墨做阴极,铁做阳极
B.电解时,在阳极上产生氢气
C.电解后得到KIO3产品的步骤有:过滤→浓缩→结晶→灼烧
D.电解中,每转移0. 6mol电子,理论上可得到0.1mol无水KIO3晶体
参考答案:D
本题解析:
本题难度:一般
4、填空题 (17分)铜在工农业生产中有着广泛的用途。
(1)配制CuSO4溶液时需加入少量稀H2SO4,其原因是 (只写离子方程式)。
(2)某同学利用制得的CuSO4溶液,进行以下实验探究。
①图甲是根据反应Fe+CuSO4=Cu+FeSO4设计成铁铜原电池,请图甲中的横线上完成标注。
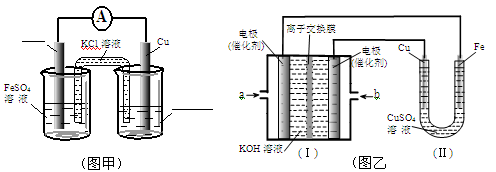
②图乙中,I是甲烷燃料电池的示意图,该同学想在II中实现铁上镀铜,则应在a处通入 (填“CH4”或“O2”),b处电极上发生的电极反应式为 ==4OH-;
若把II中电极均换为惰性电极,电解液换为含有0.1molNaCl溶液400mL,当阳极产生的气体为448mL(标准状况下)时,溶液的pH= (假设溶液体积变化忽略不计)。
(3)电池生产工业废水中常含有毒的Cu2+等重金属离子,常用FeS等难溶物质作为沉淀剂除去[室温下Ksp(FeS)=6.3×10-18mol2・L-2,Ksp(CuS)=1.3×10-36mol2・L-2]。请结合离子方程式说明上述除杂的原理:当把FeS加入工业废水中后,直至FeS全部转化为CuS沉淀,从而除去溶液中Cu2+。
参考答案:(1)Cu2++2H2O 本题解析: 本题解析:
试题分析:(1)加入稀硫酸是为了抑制Cu2+的水解;(2)图乙在Fe上镀铜,所以Fe作阴极,则连接的为燃料电池的负极,应通入CH4,b极通入O2发生还原反应:O2+4e-+2H2O =4OH-;电解池中均为惰性电极时,阳极的电极反应式为:2Cl--2e-=Cl2↑ ,阴极反应式为:2H++2e-=H2 ↑ .由电极反应式计算消耗的H+为0.04mol,则生成的OH-为0.04mol,c(OH-)=0.1mol/L,则c(H+)=10-13mol/L,pH=13;(3)应用了难溶电解质的沉淀溶解平衡,溶液中存在溶解平衡:FeS(s)  Fe 2+(aq)+ S 2-(aq),Cu2+与S 2-反应可生成溶度积更小的CuS沉淀,使得上述溶解平衡继续向右移动。 Fe 2+(aq)+ S 2-(aq),Cu2+与S 2-反应可生成溶度积更小的CuS沉淀,使得上述溶解平衡继续向右移动。
考点:盐类水解、原电池原理及计算、难溶电解质的沉淀溶解平衡。
本题难度:困难
5、填空题 从NO3-、SO42-、H+、Cu2+、Ba2+、Ag+、Cl-等离子中选出适当的离子组成电解质,采用惰性电极对其溶液进行电解。若两极分别放出气体,且体积比为1∶1,电解质的化学式可能是_________________。
参考答案:HCl(或BaCl2)
本题解析:
本题难度:一般
|