��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��������ʵ��϶����ܻ�óɹ�����[???? ]
A����pH��ֽ����Ũ������Ũ����
B������������Һ���ֶ���������������
C�������Ը��������Һ��ȥ������̼�л��е�������������
D������ˮ��ȥ�������е���������
�ο��𰸣�D
���������
�����Ѷȣ�һ��
2��ѡ���� ���÷�Һ©��������ǣ�������
A�����ͺ�ˮ
B���屽��ˮ
C���Ҵ�����ˮ
D���Ҵ�������
�ο��𰸣�A�����ͺ�ˮ���ܣ������÷�Һ�ķ������룬��A����
B
���������
�����Ѷȣ�һ��
3������� ѡ������ʵ�鷽���������ʣ������뷽����������ں����ϣ�
A����ȡ��Һ��??B�����ȷֽ�??C���ᾧ��??D����Һ��?E������?F�����˷�
��1���ӵ��ˮ��Һ����ȡ�⣺______��
��2��������غ��Ȼ��ƵĻ����Һ�л������أ�______��
��3������ˮ���͵Ļ���______��
��4������CCl4���е㣺76.75�棩�ͼױ����е㣺110.6�棩�Ļ�ϣ�______��
�ο��𰸣���1����������ˮ�л��ܼ��������ڲ�ͬ�ܼ��е��ܽ�Ȳ�ͬ����ѡ
���������
�����Ѷȣ�һ��
4��ѡ���� ��NA��ʾ�����ӵ�������ֵ������˵����ȷ����
A.1molCl2������������Ӧ����FeCl3
B.ת�Ƶĵ�������3NA
C.�ڱ�״���£�NA��ˮ������ռ�е����ԼΪ22.4L
D.7.8g Na2O2�к��������ӵ���ĿΪ0.1NA
E.������ˮ��Ӧʱ����ת����0.1NA
F.1mol�������е�ԭ������1mol�������е�ԭ����������
�ο��𰸣�CD
���������Aѡ����1molCl2������������Ӧ������ȫ�����ĸɾ�����Ԫ����ԭ����0��ȫ�����-1�ۣ���Ҫ�õ�������ĿΪ2NA������Ϊ��������ԭ��Ӧ�е�ʧ����Ҫ�غ㣬�����ܵ�ת�Ƶ�����ĿҲӦ����2NA��Bѡ����NA��ˮ�������ʵ���Ϊ1mol�����ڱ�״���£�ˮ�������壬���������Ӧ����22.4L��Cѡ���й����������������ǹ��������ӣ�7.8gNa2O2���ʵ���Ϊ0.1mol,��ô���������ӵ���ĿӦΪ0.1NA������ˮ��Ӧʱ�������Ʒ�������������ԭ��Ӧ�����������е�������ԭ��һ�����0�ۣ�һ����ɸ����ۣ�ת�Ƶ�����Ϊ0.1NA��Dѡ��������˫ԭ�ӷ��ӣ�1mol����ԭ����ĿΪ2NA��������Ϊ��ԭ�ӷ��ӣ�1mol�������е�ԭ������Ӧ��NA��
�����Ѷȣ�һ��
5��ʵ���� ��13�֣�ijѧϰС��Ϊ�о��ͼ�̬��Ԫ�����ʵĻ�ԭ�ԣ���NH3Ϊ�����������ͼʵ�飨�г��豸��ȥ��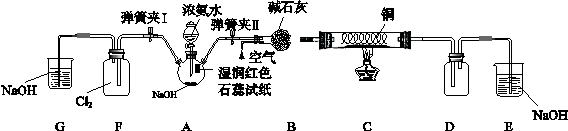 ?
?
I�����������Ժ�رյ��ɼ�I���ɼ�II����ȼ�ƾ��ƣ�ͭ˿���Ⱥ��Һ©���Ļ�����A���������B��ʱ����ͨ���������Ӧһ��ʱ���Ϩ��ƾ��ơ�
II����D������������ʱ�رյ��ɼ�II�����ɼ�I
��1����֤���а���������������??????????????????????????�������ӵ���ʽΪ????????????��
��2��C��ͭ˿��Ϩ��Ƶƺ��Ա��ֺ���˵�����з�ӦΪ????????��Ӧ������ȡ����ȡ���NH3��
C�з�Ӧ�Ļ�ѧ����ʽΪ?????????????????????????????????????????????????????????��
��3��D�в�������ɫ����Ͱ��̣��������̵Ļ�ѧ����ʽΪ��????????????????????????????
��4��F��Ҳ�����������̣�д���÷�Ӧ�з�Ӧ������ʵ���֮��n(NH3):n(Cl2)??????????????
��5���û�ѧ����ʽ����Ӧ����˵��A���ܲ�������NH3�����ԭ��?????????????????????????���Ƚ�ijʱ��A�з�Һ©����Һƽ�ⳣ��K1������ƿ����Һ��ƽ�ⳣ��K2��С��ϵ��K1???K2(�<����=����>��)��
�ο��𰸣���13�֣�
��1��A��ʪ��ĺ�ɫʯ����ֽ������?
���������
�����������1����������ˮ�Լ��Կ���ʹ��ɫʯ����ֽ����������A��ʪ��ĺ�ɫʯ����ֽ������֤���а��������������ӵ���ʽΪ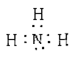 ��
��
��2��˵����Ӧ����Ϊͭ˿�������ֱ��ֺ��ȣ��÷�ӦΪ4NH3 +5O2 ??4NO + 6H2O��2NH3 +3CuO
??4NO + 6H2O��2NH3 +3CuO ?3Cu +N2+ 3H2O��
?3Cu +N2+ 3H2O��
��3��D������Ҫ��HNO3��NH3��Ӧ���ɵ�NH4NO3�����Բ������̵Ļ�ѧ����ʽΪHNO3 + NH3 = NH4NO3��
��4��F�з�����Ӧ3Cl2+8NH3=6NH4CL+N2����Ӧ������ʵ���֮��n(NH3):n(Cl2)Ϊ8:3��
��5��A�д��ڻ�ѧƽ��NH3? +? H2O NH3.H2O
NH3.H2O NH4+ ?+? OH-? ��H ��0����������ʹc(OH-)����ƽ�������ƶ���ͬʱ����������ˮ�ų������ȣ�Ҳʹƽ�������ƶ��������ܲ�������NH3���壻��ѧƽ�ⳣ��K�Ĵ�Сֻ���¶Ⱦ���������ƿ��������������ˮ�ų������ȣ���Һ�¶����ߣ���K1С��K2��
NH4+ ?+? OH-? ��H ��0����������ʹc(OH-)����ƽ�������ƶ���ͬʱ����������ˮ�ų������ȣ�Ҳʹƽ�������ƶ��������ܲ�������NH3���壻��ѧƽ�ⳣ��K�Ĵ�Сֻ���¶Ⱦ���������ƿ��������������ˮ�ų������ȣ���Һ�¶����ߣ���K1С��K2��
���������⿼�鵪Ԫ�����ʵĻ�ԭ�Լ���ѧ��Ӧƽ���֪ʶ����һ�����Ѷȣ�Ҫ������Ϥ�������֪ʶ��
�����Ѷȣ�һ��