Z
?
A.R的气态氢化物与它的含氧酸之间能发生化学反应
B.原子半径大小顺序是:Z>Y>X
C.Y、Z的单质在一定条件下均能与Fe反应
D.X、Y、Z中Z的氧化物对应的水化物的酸性最强
参考答案:AC
本题解析:
本题难度:一般
2、选择题 某元素的原子最外电子层排布是6s26p4,该元素或其化合物不可能具有的性质是
A.该元素单质可能是导体
B.该元素的最高化合价呈+6价
C.该元素能与氢气反应生成气态氢化物
D.该元素单质形成的晶体晶胞是简单立方
参考答案:C
本题解析:
本题难度:一般
3、填空题 根据X、Y、Z、W四种常见元素的下列信息,回答有关问题:
信息1:上述四种元素均为短周期元素,其原子序数依次增大,且原子核外最外层电子数均不少于2。
(1)根据信息1,X一定不是________(填序号);
A.氢
B.碳
C.氧
D.硫
信息2:上述四种元素的单质均能在足量的氧气中燃烧,生成的四种氧化物中,有两种能溶于稀硫酸,三种能溶于浓氢氧化钠溶液,氧化物的相对分子质量都大于26。
(2)这四种元素中是否有一种是铝元素________(填“是”或“否”);
信息3:向上述四种元素的单质组成的混合物中加入足量稀盐酸,固体部分溶解,过滤,向滤液中加入过量的烧碱溶液,最终溶液中析出白色沉淀。
(3)生成白色沉淀物的化学式为_________________________________________;
信息4:向上述四种元素的单质组成的混合物中加入足量烧碱溶液,固体部分溶解,过滤,向滤液中加入足量的稀盐酸,最终溶液中析出白色沉淀。
(4)生成白色沉淀物的化学式为___________________________________________。
参考答案:(1)A? (2)是? (3)Mg(OH)2? (4)H2S
本题解析:
本题难度:一般
4、填空题 (16分)Ⅰ.短周期元素X、Y、Z、W在元素周期表中的位置如图所示,其中X、Y、Z三种元素的质子数之和为21。

(1)写出W的简单离子的原子结构示意图??????????????????;
氢元素与Z形成原子个数比为1∶1的化合物,其结构式为???????????。
(2)Y的最高价氧化物对应的水化物与Y的氢化物恰好完全反应,生成物的水溶液呈酸性,其原因是(用离子方程式表示)??????????????????????????????????????????;
(3)写出Y的最高价氧化物对应水化物的浓溶液与X在加热条件下反应的化学方程式
???????????????????????????????????????????????????????????? ???????????????, ???????????????,
反应中每转移8mol 电子,消耗的还原剂质量为???????g。
(4)写出能说明Y的非金属性比Z弱的一个实验事实:?????????????????????????
Ⅱ.往1L体积不变的容器中加入0.200mol CO和1.00mol H2O(g),在t℃时反应:
CO+ H2O(g) 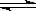 CO2+ H2达到平衡,若该反应的化学平衡常数K=1,则t℃时CO 的转化率为???????????????????。 CO2+ H2达到平衡,若该反应的化学平衡常数K=1,则t℃时CO 的转化率为???????????????????。
Ⅲ.甲醇燃料电池是一种相对理想的绿色能源,可用于电动汽车的电源;若该氢氧燃料电池以硫酸为电解质溶液,总反应为:2CH3OH + 3O2 = 2CO2+ 4H2O,则其正极的电极反应式???????????????????????????????????????????????????????????????????????
参考答案:Ⅰ(1)硫离子的结构示意图(略);H-O-O-H
(2
本题解析:
本题难度:一般
5、填空题 (10分)(1)在 H, H,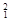 H, H,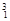 H, H,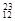 Mg, Mg,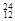 Mg, Mg,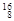 O, O, O, O,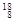 O中共有______种元素,______种原子,中子数最多的是?????。D218O的相对分子质量是______。 O中共有______种元素,______种原子,中子数最多的是?????。D218O的相对分子质量是______。
(2)人类的生活和生产活动,都离不开能源。在石油、电能、风能、煤碳、天然气、秸杆、水力、水煤气这些能源中,属于“二次能源”的(两种)是____,_????????(共1分)属于“不再生能源”的(三种)是___?,??????,???_(共1分)。
(3)化学反应的限度是当_??????_____和???????__相等,反应物和生成物的 _??????____保持不变时,所达到的一种看似???????? 的“平衡状态”。
参考答案:(1) 3, 8,Mg,22
(2)电能、水煤气,石油
本题解析:
本题难度:简单
|