微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述正确的是(???)
A.同温同压下,4Al(s)+3O2(g)===2Al2O3(s)在常温和点燃条件下的ΔH不同
B.在某反应中,当反应物具有的总能量大于生成物具有的总能量时,该反应放热,△H>0
C.已知C(s)+1/2O2(g)="CO(g);" △H =-110.5kJ・mol-1,则碳的标准燃烧热是△H =-110.5kJ・mol-1
D.新能源应具有资源丰富、可再生、无污染或少污染等特点。如太阳能、氢能、风能、地热能、潮汐能和生物质能等新能源
参考答案:D
本题解析:A:只要反应物与生成物的状态不变,焓变是不变的;B:当反应物具有的总能量大于生成物具有的总能量时,该反应放热,△H<0;燃烧热要求1mol可燃物完全燃烧生成稳定的氧化物,而本项是碳的不完全燃烧
本题难度:一般
2、选择题 已知石墨在一定条件下转化成金刚石是吸热反应,由此可能出的正确结论是
A.石墨比金刚石更稳定
B.金刚石比石墨更稳定
C.石墨转化成金刚石是物理变化
D.石墨和金刚石的结构相同
参考答案:A
本题解析:根据题意可知,石墨的能量小于金刚石的,能量越低越稳定,所以石墨稳定。金刚石和石墨都是碳的同素异形体,二者的结构不同,它们之间相互转化是化学变化,答案选A。
本题难度:一般
3、选择题 铅蓄电池的工作原理是把储藏的化学能转化为
A.太阳能
B.氢能
C.电能
D.化学能
参考答案:C
本题解析:铅蓄电池属于原电池,原电池工作原理是将化学能转化为电能;
本题难度:简单
4、选择题 标准状态下,气态分子断开l mol化学键的焓变称为键焓。已知H-H、H-O和O-O键的键焓ΔH分别为436 kJ/mol、463 kJ/mol和495kJ/mol。下列热化学方程式正确的是
A.H2O (g)= H2(g)+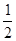 O2(g); ΔH=" -485" kJ/mol
O2(g); ΔH=" -485" kJ/mol
B.H2O (g)=H2(g)+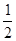 O2(g); ΔH="=+485" kJ/mol
O2(g); ΔH="=+485" kJ/mol
C.2H2(g)+ O2 (g)= 2H2O(g) ΔH =" +485" kJ/mol
D.2H2(g)+ O 2(g)=2H2O(g) ΔH =" -485" kJ/mol
参考答案:D
本题解析:
试题分析: 1mol的气态水分解产生1mol的氢气和1/2mol的氧气的能量变化是:2×463 kJ-436-1/2×495="242." 5.因此热化学方程式为H2O (g)= H2(g)+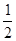 O2(g);? ΔH=" +242." 5kJ/mol。A.B错误。则若是2mol的气态水分解产生2mol的氢气
O2(g);? ΔH=" +242." 5kJ/mol。A.B错误。则若是2mol的气态水分解产生2mol的氢气
本题难度:一般
5、填空题 (14分)2SO2(g)+O2(g) 2SO3(g),反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。
2SO3(g),反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ/mol。
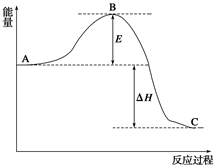
请回答下列问题:
(1)图中A、C分别表示__________、______________,E的大小对该反应的反应热有无影响?______________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?____________;
(2)图中ΔH=__________kJ/mol;
(3)如果反应速率v(SO2)为0.05 mol/(L・min),则v(O2)=________mol/(L・min)
(4)已知单质硫的燃烧热为296 kJ/mol,计算由S(s)生成3 mol SO3(g)的ΔH=_?? _。
参考答案:(1)反应物能量?生成物能量??没有影响?降低(2)-198
本题解析:
试题分析:化学反应过程中使用催化剂会降低反应的活化能,但不会影响反应的焓变;由S(s)生成3 mol SO3(g)的ΔH=-(296 kJ/mol×3+99 kJ/mol×3)=-1185kJ/mol。
本题难度:一般