微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 设氨水的pH=x,某盐酸的pH=y,已知x+y=14,且x>11。将上述两溶液分别取等体积充分混合后,所得 溶液中各离子浓度由大到小的顺序是 [???? ]
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-)
B.c(NH4+)>c(Cl-)>c(H+)>c(OH-)
C.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
D.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
参考答案:C
本题解析:
本题难度:一般
2、选择题 下列溶液中有关离子浓度的说法可能正确的是( ? )
A.NH4Cl溶液:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.Na2CO3溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-)
C.等物质的量的CH3COOH与NaOH混合溶液中:c(CH3COO-)=c(Na+)=c(H+)=c(OH-)
D.在NaHCO3溶液中:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
参考答案:D
本题解析:
本题难度:一般
3、选择题 下列说法中正确的是
A.三氧化硫的水溶液能导电,但是三氧化硫是非电解质
B.用固态的溶质配成同为1 mol/L的硝酸铵溶液和氢氧化钠溶液,立即做导电性实验,两种溶液的导电性相同
C.在相同温度下,强电解质溶液一定比弱电解质溶液的导电性强
D.在相同温度下,饱和溶液一定比不饱和溶液的导电性强
参考答案:A
本题解析:A项SO3本身不发生电离,它跟H2O反应生成的H2SO4是电解质.B项.NH4NO3溶解吸热,溶液温度较低,NaOH溶解放热,溶液温度较高.C项,强电解质溶液里离子的物质的量浓度不一定大,弱电解质溶液里离子的物质的量浓度不一定小.D项,饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液.
本题难度:困难
4、选择题 下列有关物质分类一定正确的是( )
①强电解质:氯化氢、氢氧化钡、摩尔盐
②弱电解质:草酸、纯碱、醋酸铵
③非电解质:液氨、二氧化硫、苯
④同系物:CH202、C2H402、C3H602.
A.①②③
B.①③
C.①④
D.②③
参考答案:①氯化氢、氢氧化钡、摩尔盐都是强电解质,故①正确;
②
本题解析:
本题难度:一般
5、填空题 Ⅰ.在一容积为2?L的密闭容器内加入2?mol的CO和6?mol的H2,在一定条件下发生如下反应:CO(g)+?2H2(g) CH3OH(g);ΔH????????
CH3OH(g);ΔH????????
(1)反应达到平衡时,?CH3OH的物质的量浓度可能为______。
A.0.9?mol/L?????B.1.0?mol/L???????C.1.5?mol/L??
若经过3分钟,CH3OH达到了以上浓度,则VCO=__________
该反应的化学平衡常数是____________。
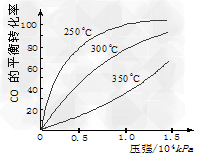
(2)?CO在不同温度下的平衡转化率与压强的关系如图所示。该反应ΔH________0(填“>”或“?<”)。实际生产条件控制在250℃、1.3×104kPa左右?,选择此条件的理由是
______________________。
Ⅱ.已知草酸是一种二元弱酸,草酸氢钠(NaHC2O4)溶液显酸性。
(1)用离子方程式解释Na2C2O4溶液显碱性的原因____________________;
(2)常温下,向10?m?L?0.01?mol・L-1?H2C2O4溶液中滴加10mL?0.01mol・L-1?NaOH溶液时,比较溶液中各种离子浓度的大小关系________________?;
(3)称取6.0g含H2C2O4・2H2O、KHC2O4和K2SO4的试样,加水溶解配成250?mL?溶液。量取两份此溶液各25?mL,分别置于两个锥形瓶中?。第一份溶液中加入2滴酚酞试液,滴加0.25mol・L-1??NaOH?溶液至20mL时,溶液由无色变为浅红色。第二份溶液滴加0.10?mol・L-1?酸性KMnO4溶液至16mL时反应完全。则原试样中H2C2O4・2H2O的的质量分数为_______?。
参考答案:Ⅰ(1)A;0.3mol・L-1・min-1?;1/16 或
本题解析:
本题难度:一般