微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (6分)某温度时,在2L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化的曲线如图所示。由图中数据分析:
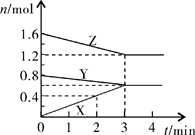
(1)该反应的化学方程式:????????????????????????????;
(2)0~2min末,X的平均反应速率为???????????????????mol・L-1・min-1;
(3)3min后图中曲线所表示的含义是???????????????????????????????????
????????????????????????????????。
参考答案:(1)Y(g)+2Z(g) 本题解析:(1)根据图像可知,反应进行到3min时,Z和Y的物质的量分别减少0.4mol、0.2mol,X的物质的量增加0.6mol。所以根据变化量之比是相应的化学计量数之比可知,方程式为Y(g)+2Z(g)
本题解析:(1)根据图像可知,反应进行到3min时,Z和Y的物质的量分别减少0.4mol、0.2mol,X的物质的量增加0.6mol。所以根据变化量之比是相应的化学计量数之比可知,方程式为Y(g)+2Z(g) 3X(g)。
3X(g)。
(2)反应速率通常用单位时间内浓度的变化量来表示,所以0~2min末,X的平均反应速率为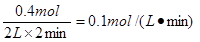 。
。
(3)根据图像可知,3min后物质的浓度不再发生变化,所以反应达到平衡状态。
本题难度:一般
2、选择题 实验测得鲜牛奶在30 ℃时6小时变质,该反应温度每升高10 ℃时反应速率增大一倍,现将鲜牛奶放在冰箱的冷藏室里,保鲜期延长为48小时,则该冰箱的冷藏室里的温度为(???)
A.-20 ℃
B.-10 ℃
C.0 ℃
D.10 ℃
参考答案:C
本题解析:将牛奶放在冰箱里,保鲜期比30 ℃条件下增大了 =8倍,则牛奶变质的反应速率应降低8倍。设30 ℃时牛奶的变质速率为v,t ℃时,牛奶变质速率为
=8倍,则牛奶变质的反应速率应降低8倍。设30 ℃时牛奶的变质速率为v,t ℃时,牛奶变质速率为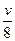 。根据题意v・
。根据题意v・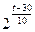 =
= ?v,则t="0" ℃。选C。
?v,则t="0" ℃。选C。
本题难度:一般
3、选择题 在373K时,把0.5mol N2O4通入体积为5 L的真空密闭容器中,立即出现棕色。反应进行到2s时,NO2的浓度为0.02mol・L-1。在60 s时,体系已达平衡,此时容器内压强为开始的1.6倍。 下列说法正确的是 [???? ]
A.前2s,以N2O4的浓度表示的平衡反应速率为0.01 mol・L-1・s-1
B.在2s时体系内的压强为开始时的1.1倍
C.在平衡时体系内含N2O4 0.25mol
D.平衡时,如果压缩容器体积,则可提高N2O4的转化率
参考答案:B
本题解析:
本题难度:一般
4、选择题 一定温度下,把2. 0体积的N2和6. 0体积的H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通,容器中发生如下反应:N2+3H2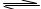 2NH3。已知平衡时NH3的浓度是c mol・L-1,现按下列四种配比作为起始物质,分别充入上述容器,并保持温度不变,则达到平衡后,NH3的浓度不为c mol・L-1的是
2NH3。已知平衡时NH3的浓度是c mol・L-1,现按下列四种配比作为起始物质,分别充入上述容器,并保持温度不变,则达到平衡后,NH3的浓度不为c mol・L-1的是
A.1.0体积的N2和3.0体积的H2
B.2.0体积的N2、6.0体积的H2和4.0体积的NH3
C.4.0体积的NH3和1.0体积的H2
D.2.0体积的NH3
参考答案:C
本题解析:在等温等压情况下的等效平衡,只要求反应物的量担按系数比转化为半边后,两反应物的量的比例符合1:3即可。
本题难度:一般
5、填空题 (6分)由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。
(1)在250C、101KPa时,3.2克甲醇(CH30H)完全燃烧生成CO2和液态水时放热72.576kJ,则能表示甲醇燃烧的热化学方程式为___________________。
(2)为探究反应原理,现进行如下实验,在体积为2 L的密闭容器中,充入2mol CO2和6mol H2,一定条件下发生反应:CO2(g)+3H2(g)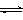 CH3OH(g)+H2O(g) △H=―49kJ/mol,测得CO2和H2O (g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) △H=―49kJ/mol,测得CO2和H2O (g)的浓度随时间变化如图所示。
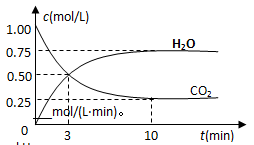
①从反应开始到平衡,氢气的平均反应速率v(H2)=__________mol/(L・min)。
②下列措施中能使n(H2O)/n(CO2)增大的是________。
A.升高温度?????????????????????? B.再充入3mol H2
C.将CH3OH (g)从体系中分离??????? D.充入He(g),使体系压强增大
参考答案:(6分)(1)CH3OH(l)+3/2O2(g)=CO2(g
本题解析:略
本题难度:简单