微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 25℃时,在等体积的①ph=0的 溶液、②0.05mol/L的
溶液、②0.05mol/L的 溶液、③ph=10的
溶液、③ph=10的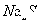 溶液、④pH=5的
溶液、④pH=5的 溶液中,发生电离的水的物质的量之比是
溶液中,发生电离的水的物质的量之比是
A.1:10:10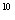 :10
:10
B.1:5:5 10
10 :5
:5 10
10
C.1:20:10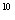 :10
:10
D.1:10:10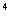 :10
:10
参考答案:A
本题解析:
正确答案:A
①中pH=0的H2SO4中c(H+)="1.0" mol・L-1,c(OH-)=1.0×10-14mol・L-1,水电离程度为1.0×10-14mol・L-1。②中c(OH-)="0.1" mol・L-1,c(H+)=1.0×10-13mol・L-1,水电离程度为1.0×10-13mol・L-1。③中c(OH-)=1.0×10-4mol・L-1,水的电离程度为1.0×10-4mol・L-1。④中c
本题难度:一般
2、填空题 (3分)写出下列物质的电离方程式:
(1)H2CO3
(2)NaHSO4
(3) NH3・H2O
参考答案:(3分)(1)H2CO3 本题解析:考查电离方程式的书写。化学式和离子符号表示电离过程的式子,称为电离方程式。在书写时需要注意,强电解质用等号,弱电解质一律用可逆号,多元弱酸分步电离,多元弱碱一步电离。强酸的酸式盐一步电离。弱酸的酸式盐分步电离,第一步不可逆,以后步步可逆,且一步比一步的电离程度小。
本题解析:考查电离方程式的书写。化学式和离子符号表示电离过程的式子,称为电离方程式。在书写时需要注意,强电解质用等号,弱电解质一律用可逆号,多元弱酸分步电离,多元弱碱一步电离。强酸的酸式盐一步电离。弱酸的酸式盐分步电离,第一步不可逆,以后步步可逆,且一步比一步的电离程度小。
本题难度:一般
3、选择题 用pH均为2的盐酸和醋酸溶液,分别中和等体积、等物质的量浓度的氢氧化钠溶液,当氢氧化钠恰好被完全中和时,消耗盐酸和醋酸溶液的体积分别为Vl和V2,则Vl和V2的关系正确的是
[???? ]
A.V1>V2
B.V1<V2
C.V1=V2
D.V1≤ V2
参考答案:A
本题解析:
本题难度:一般
4、选择题 将C(H+)=1×10-2mol・L-1的CH3COOH和HNO3溶液分别稀释100倍,稀释后两溶液的H+的物质的量浓度分别为a和b,则a和b的关系为[???? ]
A.a>b
B.a<b
C.a=b
D.不能确定
参考答案:A
本题解析:
本题难度:一般
5、选择题 下列叙述正确的是( )
A.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊试液呈红色
B.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2
C.pH=2与pH=1的硝酸中c(H+)之比为10:1
D.向0.1mol/L的氨水中加入少量醋酸铵固体,则溶液中
c(OH-)
c(NH3?H2O)
增大
参考答案:A.pH=11的NaOH溶液与pH=3的醋酸溶液中,醋酸浓度
本题解析:
本题难度:简单
|