微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 A、B、C、D四种物质皆易溶于水,且在水溶液中存在如下化学平衡,加水稀释后,平衡向正反应方向移动的是……( )
A、A+B C+D ????B、A+H2O
C+D ????B、A+H2O C+D ????C、A+B
C+D ????C、A+B C+H2O ????D、A+2B+H2O
C+H2O ????D、A+2B+H2O C
C
参考答案:B
本题解析:首先注意到所加水属于纯液体,固体和纯液体的量的增减对化学平衡移动是没有影响的,但加水可以改变其它物质的浓度,从而影响化学平衡。A选项,加水稀释A、B、C、D均为相同倍数,故平衡不移动。B选项,A与C、D各稀释相同倍数,C、D为生成物两种浓度的减小,大于A物质(反应物)浓度的减小,利用勒夏特列原理,平衡右移。同样道理,C、D两个选项,平衡均左移。
本题难度:一般
2、选择题 相同温度下,体积均为0.5 L的两个恒容密闭容器中发生可逆反应:
2XY2(g)+Y2(g)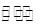 2XY3(g),?
2XY3(g),?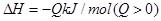
实验测得反应在起始、达到平衡时的有关数据如下表所示:
容器
| 起始时各物质物质的量/mol
| 达平衡时体系能量的变化
|
编号
| XY2
| Y2
| XY3
|
①
| 2
| 1
| 0
| 放热0.25QkJ
|
②
| 1.2
| 0.6
| 0.8
| ?
下列叙述不正确的是
A.达到平衡时,①和②两容器中气体的平均相对分子质量相同
B.容器②中反应达到平衡时放出的热量为0.15 Q kJ
C.达到平衡时,两个容器中Y2的物质的量浓度均为1.5 mol・L-1
D.若容器①的其他条件不变,只增加1mol稀有气体,则达到平衡时放出的热量等于0.25 Q kJ
参考答案:B
本题解析:由容器①放热量可知,平衡时各物质消耗量(生成量)为:XY2:0.5mol, Y:0.25mol, XY3:0.5mol,剩余量为:XY2:1.5mol, Y:0.75mol, XY3:0.5mol,则平衡时浓度为:XY2:3mol/L, Y:1.5mol/L, XY3:1mol/L,K值为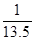 。C描述 。C描述
本题难度:一般
3、选择题 对温度与反应方向的关系,下列判断不正确的是
[???? ]
A.△H<0,△S>0,所有温度下反应自发进行
B.△H>0,△S>0,所有温度下反应自发进行
C.△H<0,△S<0,低温下反应自发进行
D.△H>0,△S<0,所有温度下反应不能自发进行
参考答案:B
本题解析:
本题难度:简单
4、选择题 已知工业上真空炼铷的反应方程式为:2RbCl + Mg  MgCl2 + 2Rb(g),对于此反应,能够进行正确解释的是 ( ) MgCl2 + 2Rb(g),对于此反应,能够进行正确解释的是 ( )
A.铷比镁金属性强
B.氯化镁比氯化铷难溶
C.高温下,镁离子得电子能力比铷离子弱
D.铷的沸点比镁低,当把铷蒸气抽走时,平衡向右反应方向移动
参考答案:D
本题解析:略
本题难度:一般
5、选择题 在固定体积的密闭容器中,发生:N2(g)+3H2(g) 2NH3(g)DH=-92.2 kJ・mo1-1 ,下图表示在时间t0~t7中反应速率与反应过程的曲线图,则容器内氨的百分含量最高的一段时间是(只改变单一的条件) 2NH3(g)DH=-92.2 kJ・mo1-1 ,下图表示在时间t0~t7中反应速率与反应过程的曲线图,则容器内氨的百分含量最高的一段时间是(只改变单一的条件)
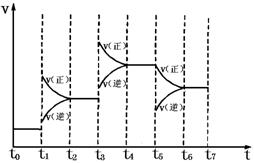
A.t0~t1
B.t2~t3
C.t4~t5
D.t6~t7
参考答案:C
本题解析:略
本题难度:简单
|