��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ������ijЩ������������ɵĻ�����ڻ�ѧ�ϳ�Ϊ���ȼ����û�����ڸ����������ܷ����û���Ӧ��Ϊȷ��ij���ȼ���Ʒ������������������ɣ��ֱ��������ʵ�飺
��1����ȡ10.7g����Ʒ�������м���������NaOH��Һ��������ɵ����壨��״������ͬ�����Ϊa?L����Ӧ�Ļ�ѧ����ʽ��______����Ʒ����������������______���ú�a�ı���ʽ��ʾ����
��2����ȡͬ��������Ʒ���ڸ�����ʹ��ǡ�÷�Ӧ����a=______L���÷�Ӧ�Ļ�ѧ����ʽ��______��
��3������2���з�Ӧ������ȴ�����������ᣬ������ɵ��������Ϊb?L���������루1������������������a��b______��
�ο��𰸣���1������NaOH��Ӧ�Ļ�ѧ����ʽΪ2Al+2NaOH+2H
���������
�����Ѷȣ�һ��
2��ѡ���� ���й������Ͻ��˵���д������?????????????????????????????????????????��???��
A��þ���Ͻ������ŨH2SO4�жۻ�
B��þ���Ͻ����������ܱ��ռʴ
C��þ���Ͻ���һ�ֻ������ȴ������۵��
D��������Һ�ױ����������Ͻ�Ӧ���ۼ��㸲��������
�ο��𰸣�A
�����������
�����Ѷȣ���
3��ѡ���� ���ֱ���������ϡ���������������Һ��Ӧ����������Ӧ�ų�����������ͬ״����������ʱ����Ӧ�����ĵ������NaOH���ʵ���֮��Ϊ
A��1:1
B��3:1
C��3:2
D��1:3
�ο��𰸣�C
���������
�����������Ӧ���йط���ʽΪ���������2Al+6HCl��2AlCl3+3H2��������NaOH��Һ��2Al+2NaOH+2H2O��2NaAlO2+3H2�����������ɵ����������ʵ���Ϊ3mol�����ݷ���ʽ����NaOH��HCl�����ʵ������Ӷ�������������ƺ��Ȼ������ʵ�����֮�ȡ������ɵ����������ʵ���Ϊ3mol����
2Al+6HCl��2AlCl3+3H2��
6mol??????3mol
2Al+2NaOH+2H2O��2NaAlO2+3H2��
2mol?????????3mol
�����Ѷȣ�һ��
4��ѡ���� ���ơ�����������A1g��Ͷ��һ������ˮ�г�ַ�Ӧ������û��ʣ�࣬���ռ�����״���µ�����7.84L������Һ����μ���Ũ��Ϊ2mol?L-1��H2SO4��Һ����100mlʱ��ɫ�����ﵽ���������������H2SO4��Һ��������H2SO4��Һ�����Ϊxmlʱ����ǡ����ʧ����������Һ�������յù���A2g�����й�ϵʽ�в���ȷ���ǣ�������
A�������ﵽ�����ʱ��Һ�е�����ΪNa2SO4��NaHSO4
B��x=75ml
C��A1=11.9
D����ɫ���������Ϊ7.8g
�ο��𰸣�A�����ơ��������Ͷ��ˮ�У������ķ�ӦΪ2Na+2H2O�T2
���������
�����Ѷȣ���
5������� ij��ѧ��ȤС��ģ�ҵ�ϴ���������Ҫ�ɷ���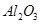 ����
����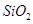 ��
��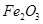 �����ʣ�����ȡ�������Ĺ�����ʵ�飬�������£�
�����ʣ�����ȡ�������Ĺ�����ʵ�飬�������£�
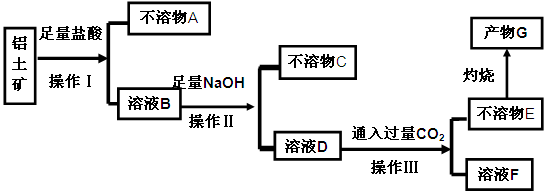
��ش��������⣺
��1�������������Ϊ???????????��
��2����֤��ҺB���Ƿ���Fe3+�ķ�����????????????????????????????????????????????��
��3��������A��????????(�ѧʽ)��д��D��E��Ӧ�����ӷ���ʽ??????????????????????��
��4��˵����ҺF�к�̼Ԫ�����ʵ�һ����;???????????????????????????????????��
�ο��𰸣���1�����ˣ�2�֣�
��2��ȡ������ҺB���Թ��У�������
���������
�������������������������е�Al2O3��Fe2O3��MgO�ܺ����ᷴӦ����SiO2�����ܽ⣬��������A��SiO2���������ǹ��ˣ����õ���ҺB���Ȼ������Ȼ������Ȼ�þ�Լ����������ᣬ�����мӹ������ռ���ò�����CΪMg(OH)2? Fe(OH)3��������Ҳ�ǹ��ˣ� ������ҺD����Ҫ�ɷ�Ϊƫ�����ƣ�ͨ�����CO2�Ļ�ѧ����ʽΪNaA1O2+CO2+H2O=Al(OH)3 ��+NaHCO3��������Ҳ�ǹ��ˣ������Ƿ��룬������EΪAl(OH)3�����պ����ɲ���GΪAl2O3����1�����������
�����Ѷȣ�һ��