微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
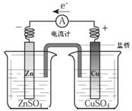
1、选择题 中学化学教材中,常借助于图像这一表现手段清晰地突出实验装置的要点、形象地阐述化学过程的原理。下列有关化学图像表现的内容错误的是

 ?
?
A.铜锌原电池
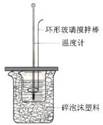
B.中和热测定装置
C.离子交换膜法电解原理
D.氨的制取装置
参考答案:A
本题解析:
试题分析:从装置中看以看到,锌做负极,放电,失去电子,所以电子从锌电极流出,所以A错。故选A。
点评:对中学化学教材中常见的的实验装置的要点识记准确就可以完成此类试题。
本题难度:简单
2、实验题 (12分)酸碱中和滴定是中学化学常见实验。
某同学欲测定某浓硫酸样品的物质的量浓度,进行了以下实验操作:
A.冷却至室温后,在100mL容量瓶中定容配成100mL稀硫酸。
B.量取20.00mL稀硫酸于锥形瓶中并滴入几滴指示剂。
C.将酸式滴定管和碱式滴定管 用蒸馏水洗涤干净,并用各待盛溶液润洗。
用蒸馏水洗涤干净,并用各待盛溶液润洗。
D.将物质的量浓度为1.50mol・L-1标准NaOH溶液装入碱式滴定管,调节液面记下读数V1。
E.继续滴定至终点,记下读数为V2。
F.在锥形瓶下垫一张白纸,把锥形瓶移到碱式滴定管下小心滴入NaOH标准溶液,边滴边摇动锥形瓶。
G.量取浓硫酸样品5mL,在烧杯中用蒸馏水溶解。
H.重复以上实验。
请回答下列问题:
(1)操作步骤的顺序为 → A→ → →D→ → → H(用字母填写)。
(2)量取5mL浓硫酸的仪器是 ;量取20.00mL稀硫酸的仪器是 。
(3)选用的指示剂是 。
(4)判断到达滴定终点的现象是 。
(5)下表是实验测得的有关数据:
滴定
序号
| 待测稀硫酸
的体积(mL)
| 所消耗NaOH标准溶液液的体积(mL)
|
V1
| V2
|
①
| 20.00
| 0.50
| 22.60
|
②
| 20.00
| 6.00
| 27.90
请计算出该浓硫酸样品的浓度为 mol・L-1(不必写出计算过程)。
参考答案:
 本题解析:略 本题解析:略
本题难度:一般
3、实验题 在呼吸面具和潜水艇中可用过氧化钠作供氧剂,某课外活动小组设计了如下实验装置,以证明过氧化钠可作供氧剂。装置A、B、C中盛装的试剂,可供选择的为:饱和NaHCO3溶液、CaCO3固体、NaOH溶液、1.95 g Na2O2固体。据下述装置回答问题
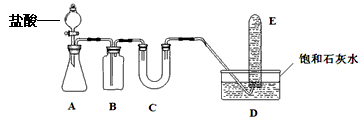
(1)A中发生反应的离子方程式为_________________。
(2)B瓶的作用是_________________,反应的离子方程式_________________。
(3)若D中的石灰水出现出现轻微白色浑浊,请说明原因:_______________________。
(4)反应完毕时,若测得E中的集气瓶收集到的气体为250 mL,又知氧气的密度为1.43g/L,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值_________(答大或小),相差约_______mL(取整数值,所用数据均在标准状况下测定),这是由于 ______________________。
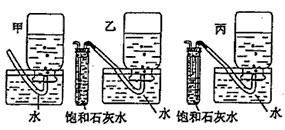
(5)为了使装置D部分更安全、合理,可将装置D改为下列________装置(用甲、乙、丙回答)
(6)实验完毕,欲测定C中固体混合物含Na2CO3的质量分数,实验步骤如下,完成以下实验步骤中的空白。若称取a g C中固体溶于一定量的水中,加入足量BaCl2溶液;过滤;___________;___________;称量得bg固体,则Na2CO3的质量分数为___________。
参考答案:(1)CaCO3 + 2H+ == Ca2+ + CO2↑+
本题解析:
本题难度:一般
4、选择题 配制一定物质的量浓度的NaOH溶液,下列情况,会使配制的结果偏高的是
A.用滤纸称量NaO H固体 H固体
B.未洗涤烧杯和玻璃棒
C.容量瓶中原来含有少量蒸馏水
D.定容时俯视刻度线观察液面
参考答案:D
本题解析:略
本题难度:一般
5、实验题 某科研小组用MnO2和浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理。
(1)请完成SO2与过量NaOH溶液反应的化学方程式:
SO2+2NaOH==?________________________。
(2)反应Cl2+Na2SO3+2NaOH===2NaCl+Na2SO4+H2O中的还原剂为__________。
(3)吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl-、OH-和SO42-。
请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气中CO2的影响)
①提出合理假设。
假设1:只存在SO32-;
假设2:既不存在SO32-,也不存在ClO-;
假设3:____________。
②设计实验方案,进行实验。请在表格中写出实验步骤以及预期现象和结论。限选实验试剂:3?mol/L?H2SO4、1?mol/L?NaOH、0.01?mol/L?KMnO4、淀粉-KI溶液、紫色石蕊试液。

参考答案:(1)Na2SO3+H2O
(2)Na2S![]()
本题解析:
本题难度:一般
|