微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (5分)已知某溶液中只存在OH-、H+、CH3COO-、Na+四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
①c(Na+)>c(CH3COO-)>c(OH-)>c(H+)。
②c(CH3COO-)=c(Na+)>c(H+)=c(OH-)
③c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
④c(CH3COO-)>c(Na+)> c(OH-) > c(H+)
(1)若溶液中只溶解了一种溶质,则该溶质是???????,上述四种离子浓度的大小顺序为??????(填编号)。
(2)若上述关系中③是正确的,则溶液中的溶质为????????。
(3)若该溶液是由体积相等的氢氧化钠溶液和醋酸溶液混合而成,且恰好呈中性,则混合前两溶液的物质的量浓度大小关系为c(NaOH)??????c(CH3COOH)(填“大于”“小于”或“等于”,下同),混合前酸中c(H+)和碱中c(OH-)的关系是c(H+)?????c(OH-)。
参考答案:(10分)(1)醋酸钠?①
(2)CH3COONa和C
本题解析:略
本题难度:简单
2、填空题 氧化铁在工业上具有广泛的应用。
I.据报道,一定条件下利用FeO2与甲烷反应可制取“纳米级”的金属铁。其反应如下:
Fe2O3(s)+3CH4(g)=2Fe(s)+3CO(g)+6H2(g) △H>0
(1)若反应在2L的密闭容器中进行,5min后达到平衡,测得反应生成Fe的质量为l.12g。则该段时间内CH4的平均反应速率为 ________________。
(2)反应达到平衡后,保持其他条件不变,仅改变某一相关元素,下列说法正确的是___(选填序号)。
a.若加入催化剂,v正增大,平衡向右移动
b.若温度升高,平衡常数K减小
c.若增大Fe2O3的量,平衡向右移动
d.若从反应体系中移走部分CO,可提高CH4的转化率
Ⅱ.工业上利用硫铁矿烧渣(主要成分为Fe2O3、A12O3、SiO2等)为原料提取Fe2O3,工艺
流程如下:试回答下列问题:
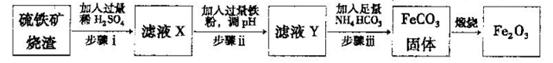
(3)步骤i烧渣中A12O3溶解的离子方程式为________________。
(4)步骤i、
参考答案:
本题解析:
本题难度:困难
3、选择题 取一定量的PbI2固体用蒸馏水配成饱和溶液,量取25.00mLPbI2饱和溶液,分次慢慢加入交换柱,进行如下离子交换反应:Pb2+(aq)+2R-H(s)=R2Pb(s)+2H+(aq),用洁净的锥形瓶接流出液,待溶液流出后,再用蒸馏水淋洗树脂至流出液呈中性,将洗涤液一并放在锥形瓶中,加入指示剂,用0.0025mol/LNaOH溶液滴定,当达到滴定终点时,用去氢氧化钠溶液20.00mL.结合上述实验数据(已知lg2=0.3),下列有关说法正确的是( )
A.常温下,0.0025mol/LNaOH溶液?pH=11.4
B.在温度不变时,向PbI2饱和溶液中加入少量硝酸铅浓溶液,PbI2的Ksp减小
C.温度不变,T时刻,向PbI2饱和溶液中加入少量KI浓溶液,离子浓度变化如图所示
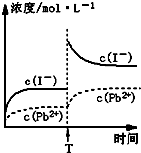
D.本次实验测得的t℃PbI2的Ksp=4×10-9
参考答案:A、常温下,0.0025mol/LNaOH溶液中c(OH-)
本题解析:
本题难度:一般
4、选择题 要使工业废水中的重金属离子Pb2+沉淀,可用硫酸盐、碳酸盐、硫化物等作沉淀剂,
已知Pb2+与这些离子形成的化合物的溶解度如下:
化合物
| PbSO4
| PbCO3
| PbS
|
溶解度/g
| 1.03×10-4
| 1.81×10-7
| 1.84×10-14
由上述数据可知,选用的沉淀剂最好为
A.硫化物???????? B.硫酸盐????? C.碳酸盐?????? D.以上沉淀剂均可
参考答案:A
本题解析:
试题分析:根据溶度积常数可知,硫化铅的溶度积常数最小,所以最好的沉淀剂是硫化物,答案选A。
点评:对于组成和结构相似的化合物,其溶度积常数越小,沉淀时需要的离子浓度越小。据此可以判断和计算。
本题难度:一般
5、选择题 工业制氯化铜时,是将浓盐酸用蒸汽加热至80 ℃左右,慢慢加入粗制氧化铜粉(含杂质氧化亚铁),充分搅拌使之溶解,反应如下:CuO+2HCl====CuCl2+H2O,FeO+2HCl====FeCl2+H2O。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀,pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀。
为除去溶液中的Fe2+,可以采用的方法是(??? )
A.直接加碱,调整溶液pH≥9.6
B.加纯铜粉,将Fe2+还原出来
C.通入适量Cl2,再加碱调整溶液的pH为4
D.直接加铁粉将Cu2+还原出来
参考答案:C
本题解析:由Fe3+、Fe2+、Cu2+完全沉淀的pH大小可知,应先将Fe2+氧化为Fe3+,再加碱调整溶液的pH生成Fe(OH)3沉淀,从而实现Fe2+和Cu2+分离。
本题难度:简单
|