微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)=Si(s)+4HCl(g) ΔH=+Q kJ・mol-1(Q>0),某温度、压强下,将一定量的反应物通入密闭容器进行以上的反应(此条件下为可逆反应),下列叙述正确的是( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol,则达到平衡时,吸收热量为Q kJ
C.反应至4 min时,若HCl的浓度为0.12 mol・L-1,则H2的反应速率为0.03 mol・L-1・min-1
D.当反应吸收热量为0.025 Q kJ时,生成的HCl通入100 mL 1 mol・L-1的NaOH溶液恰好反应
参考答案:D
本题解析:该反应为体积增大的反应,增大压强平衡左移,SiCl4转化率减小,A错;该反应为可逆反应,不能实现完全转化,放出的热量一定小于QkJ,B错;反应至4 min时,HCl的浓度为0.12 mol・L-1,表示的反应速率为:v(HCl)=0.03 mol・L-1・min-1,换算为v(H2)=0.015 mol・L-1・min-1,C错;当吸热0.025 Q kJ时,说明反应的SiCl4为0.025 mol,生成HCl 0.1 mol,其与100 mL 1 mol・L-1的NaOH恰好反应,D正确。
本题难度:一般
2、填空题 (16分)影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。
实验一:他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol・L-1、2 mol・L-1、18.4 mol・L-1)设计实验方案来研究影响反应速率的因素。甲同学的实验报告如下表:
实验步骤
| 现象
| 结论
|
①分别取等体积的2 mol・L-1的硫酸于试管中
| 反应速率Mg>Fe,Cu不反应
| 金属的性质越活泼,反应速率越快
|
②____________
| ?
| 反应物浓度越大,反应速率越快
(1)甲同学表中实验步骤②为_________________________________________。
(2)甲同学的实验目的是_____________;要得出正确的实验结论,还需控制的实验条件是____________。乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行定量实验。
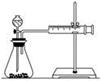
(3)乙同学在实验中应该测定的数据是___________________________________________________。
(4)乙同学完成该实验应选用的实验药品是________,该实验中不选用某浓度的硫酸,理由是___________。
实验二:已知 2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(5)针对上述实验现象,丙同学认为KMnO4与H2C2O4反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是______________的影响。
(6)若用实验证明你的猜想,除高锰酸钾酸性溶液、草酸溶液外,还需要选择的试剂最合理的是________(填字母)。
A.硫酸钾 B.硫酸锰???????????? C.二氯化锰??????????????????D.水
参考答案:(1)向等体积浓度分别为 0.5 mol/L、2 mol/L
本题解析:
试题分析:(1)甲同学表中实验步骤②为向等体积浓度分别是0.5 mol/L、2 mol/L的硫酸中加入投入大小、形状相同的Fe或者Mg。发现:同一种金属在不同浓度的硫酸中发生反应时,浓度的大的速率快。(2)甲同学的实验目的是研究金属(或反应物)本身的性质与反应速率的关系。要得出正确的实验结论,还需控制的实验条件是反应温度应该相同,这样才能形成对照实验。(3)乙同学在实验中应该测定的数据是相同时间内产生气体的体积的多少或者产生相同体积的气体所需要的时间的长短。若相同的时间内产生的气体体积越大,则反应
本题难度:一般
3、选择题 下列反应能瞬间完成的是(???)
A.硝酸见光分解
B.硝酸银溶液与盐酸的反应
C.漂白粉失效
D.二氧化硫被氧化为三氧化硫
参考答案:B
本题解析:电解质在溶液中进行的反应,一般瞬间即可完成。
本题难度:简单
4、选择题 通过控制或改变反应条件可以加快、减缓甚至阻止反应的进行,使化学反应有利于人类的生存和提高生活质量。下列各图所示的措施中,能加快化学反应速率的是
[???? ]
A. 
B. 
C. 
D. 
参考答案:C
本题解析:
本题难度:一般
5、实验题 “碘钟”实验中,3I-+S2O82-=I3-+2SO42-的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表
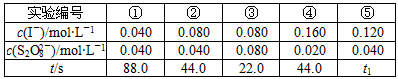
回答下列问题:
(1)该实验的目的是______________________________。
(2)显色时间t1=__________________。
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间
t2的范围为__________(填字母)。
A.<22.0 s B.22.0 s~44.0 s C.>44.0 s D.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是__________________。
参考答案:(1)研究反应物I-与S2O82-的浓度对反应速率的影响
本题解析:
本题难度:一般
|