微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关溶液中微粒浓度关系的叙述正确的是( )。
A.向0.1 mol・L-1NH4Cl溶液中通入一定量氨气后:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.溶有等物质的量NaClO、NaHCO3的溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-)
C.向CH3COONa溶液中滴加稀盐酸至中性,所得溶液中:c(Cl-)>c(Na+)>c(CH3COOH)
D.等物质的量浓度CH3COOH溶液和CH3COONa溶液等体积混合,所得溶液中:c(CH3COOH)+2c(OH-)=2c(H+)+c(CH3COO-)
参考答案:B
本题解析:阴离子总浓度不可能大于阳离子总浓度,不符电荷守恒,A错误。由NaClO的物料守恒有,c(Na+)=c(HClO)+c(ClO-),由NaHCO3的物料守恒有c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-),由于两者等物质的量,则两溶液中c(Na+)相等,B正确。由电荷守恒及溶液呈中性有c(Na+)=c(Cl-)+c(CH3COO-),则c(Na+)>c(Cl-),由CH3COONa的物料守恒有c(Na+)=c(CH3COOH)+c(CH3COO-),得c(Cl-)=c(CH3COOH),
本题难度:一般
2、选择题 欲使0.1 mol・L-1的NaHCO3溶液中c(H+)、c(CO32-)、c(HCO3-)都减小,其方法是( )
A.通入CO2
B.加入NaOH固体
C.通入HCl
D.加入饱和石灰水溶液
参考答案:D
本题解析:在NaHCO3溶液中存在如下平衡: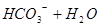 ?
?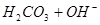 ,
, 本题难度:一般
本题难度:一般
3、选择题 在NH4Cl溶液中,各种离子浓度大小的比较,正确的是()
A.c(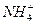 )>c(Cl-)>c(H+)>c(OH-)
)>c(Cl-)>c(H+)>c(OH-)
B.c(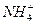 )=c(Cl-)>c(H+)>c(OH-)
)=c(Cl-)>c(H+)>c(OH-)
C.c(Cl-)>c(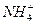 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
D.c(Cl-)>c(OH-)>c(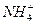 )>c(H+)
)>c(H+)
参考答案:C
本题解析:NH4Cl溶于水后发生水解: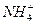 +H2O
+H2O NH3・H2O+H+,使得:c(Cl-)>c(
NH3・H2O+H+,使得:c(Cl-)>c( 本题难度:简单
本题难度:简单
4、填空题 物质的量浓度均为0.1mol/L的下列溶液:①KNO3 、②Na2CO3 、③NaHCO3 、④NaHSO4 、⑤CH3COOH、⑥NaOH、⑦Ba(OH)2 、⑧NH4Cl,pH由大到小的顺序为:
???????????????????????????????????????????????(填数字代号)
参考答案:76231854
本题解析:略
本题难度:简单
5、选择题 电解质溶液有许多奇妙之处,你只有深入思考,才能体会到它的乐趣。下列关于电解质溶液的叙述中正确的是
A.Na2CO3、NaHCO3两种盐溶液中,离子种类不相同
B.常温下,1mol/L的CH3COOH溶液与1mol/L的NaOH溶液等体积混合,所得混合液中:c(Na+) >c(CH3COO-) >c(H+)>c(OH-)
C.物质的量浓度相同的NH4Cl和NH4HSO4两种溶液中,c(NH4+)前者小于后者
D.常温下,某溶液中有水电离出的c(H+)=10-51mol・L-1,则此溶液可能是盐酸
参考答案:C
本题解析:
试题分析:A、的Na2CO3、NaHCO3两种盐溶液,阴离子都是 CO32-,HCO3-,OH-,故A错误;B、1 mol?L-1的CH3COOH溶液与1 mol?L-1的NaOH溶液混合,等体积混合,溶液呈碱性,故B错误;C、NH4HSO4溶液中,H+抑制NH4+水解,故C正确;D、常温下,水的离子积为10-14,水电离出的c(H+)=c(OH-)=10-7,酸或碱的溶液抑制水的电离,该溶液中c(H+)=10-5mol?L-1,水的电离程度程度,则此溶液不可能是盐酸,可能是强酸弱碱盐,故D错误.
本题难度:一般