微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 物质A~E中均含某种元素,都是中学化学中常见的物质,它们可发生如图所表示的反应(除A~E外的其它物质已略去):

(1)写出相应物质的类别:
| B
| C
| D
|
类别
|
|
|
(2)在以上反应中(用序号填空):
属于氧化还原反应的是 ;属于复分解反应的是 。
(3)写出反应③和⑦的离子方程式: : 。
参考答案:(1)(共3分)
B
C
本题解析:略
本题难度:一般
2、选择题 下列物质中,互为同素异形体是( )
A.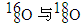
B.H2O 与H2O2
C.O2与O3
D.液氯与氯水
参考答案:C
本题解析:A不是,应该是同位素。
B不是,两者属于不同的化合物。
C是,由同种元素构成的不同单质。应该选C。
D不是,液氯是单质,氯水是混合物。
本题难度:一般
3、填空题 (6分)已知反应:
①SO2+2NaOH=Na2SO3+H2O
②SO2+2H2S=3S↓+2H2O
③SO2+Br2+H2O=H2SO4+2HBr
(1)将③反应中的反应物和生成物化学式填入下表。(每个格子只填一种)
类型
| 酸性氧化物
| 电解质
| 非电解质
| 化学式
|
|
|
(2)从①反应后的溶液中获取Na2SO3晶体,需进行的操作是 ;
从②反应后的溶液中获取S单质,需进行的操作是 ;
从③反应中提取剩余的Br2,需进行的操作是 。
参考答案:(6分)(1)
化学式
SO2
H2O或H
本题解析:
试题分析:(1)SO2+Br2+H2O=H2SO4+2HBr反应中,SO2是酸性氧化物,能与氢氧化钠反应生成盐和水;酸、碱、盐、水、部分活泼金属氧化物都是电解质,所以H2O或H2SO4或HBr;SO2是非电解质;
(2)从Na2SO3溶液中中获取Na2SO3晶体,从溶液中得到易溶的固体的方法是蒸发,所以从①反应后的溶液中获取Na2SO3晶体,需要进行蒸发操作;S单质不溶于水,将液体与不溶于液体的固体分离用过滤,所以从②反应后的溶液中获取S单质,需进行的操作是过滤;溴不易溶于水,易溶于四氯化碳,利用物质溶解性的不同分离物质用萃取,所以从③反应中提取剩余的Br2,需进行的操作是萃取。
考点:考查酸性氧化物、电解质、非电解质的判断,混合物分离方法的判断
本题难度:一般
4、选择题 实验室用下列溶质配制一种混合溶液,已知溶液中2c(K+)=2c(Cl-)=c(Na+)=2c(SO42-),则其溶质可能是
A.NaCl K2SO4
B.KCl Na2SO4 NaCl
C.NaCl K2SO4 Na2SO4
D.K2SO4 KCl Na2SO4
参考答案:C
本题解析:
试题分析:根据溶液的电中性可知,c(K+)+c(Na+)=c(Cl-)+2c(SO42-),所以根据已知的离子浓度大小关系可知,选项C有可能的,其余都不可能,答案选C。
考点:考查根据离子浓度大小判断溶液中溶质
本题难度:一般
5、选择题 下列各组物质中,前者为弱电解质,后者为强电解质的是
A.硫酸钡,硫酸
B.醋酸,醋酸钠
C.氨气,氯化铵
D.氯化钠,酒精
参考答案:B
本题解析:
试题分析:A.硫酸钡和硫酸均为强电解质,A错误;B.醋酸是弱电解质,醋酸钠属于盐,水溶液中能完全电离,是强电解质,B正确;C.氨气是非电解质,氯化铵为强电解质,C错误;D.氯化钠和酒精分别为强电解质和非电解质,D错误.答案选B.
考点:强电解质和弱电解质
本题难度:一般
|
|