微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 根据下表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是
化学式
| 电离常数
|
HClO
| Ka=3×10-18
|
H2CO3
| Ka1=4.3×10-7
|
Ka2=5.6×10-11
A.c(HCO3-)>c(ClO-)>c(OH-)
B.c(ClO-)>c(HCO3-)>c(H+)
C.c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)
D.c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+c(OH-)
参考答案:A
本题解析:
试题分析:从表达数据可以知道,酸性:H2CO3>HClO>HCO3-,那么等浓度的NaClO、NaHCO3混合溶液中,ClO-的水解程度比HCO3-大,ClO-和HCO3-水解使得溶液显碱性,故c(HCO3-)>c(ClO-)>c(OH-),A对,B错;C是物料守恒,应该是:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+ c(CO32-),C错;D是电荷守恒,应该是c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+c(OH-) + 2c(CO32-),D错。选A。
考点:酸性强弱比较、盐类水解、离子浓度的大小比较。
本题难度:一般
2、选择题 常温下,下列物质的水溶液,其pH大于7的是( ) A.Na2SO4
B.Na2CO3
C.KCl
D.NH4NO3
参考答案:B
本题解析:
本题难度:简单
3、选择题 实验中在对某种样品进行检验时,加入试剂顺序的不同对最后结果的判断具有很大影响。某样品中可能含有SO42-,实验中加入试剂种类和顺序正确的是( B )
A.BaCl2溶液,稀盐酸 B.稀盐酸,BaCl2溶液
C.BaCl2溶液,稀硝酸 D.稀硝酸,BaCl2溶液
参考答案:B
本题解析:A、C、D中分别难排除银离子、银离子、亚硫酸根等的干扰
本题难度:一般
4、选择题 在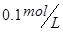 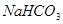 溶液中,下列关系中不正确的是 溶液中,下列关系中不正确的是
A.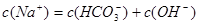
B.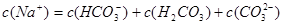
C. -c(CO32-) -c(CO32-)
D.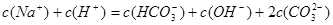
参考答案:A
本题解析:略
本题难度:一般
5、填空题 (8分)⑴ 现有0.1mol・l-1的纯碱溶液,试用pH试纸测定溶液的pH,其正确的操作 。
⑵ 欲使0.1mol-1Na2CO3溶液中c(Na+)=2 c(CO32-),应采取的措施是 ( )
A.加少量盐酸 B.加适量的KOH C.加适量的水 D.加适量的NaOH
⑶ 为证明盐的水解是吸热的,四位同学分别设计了如下方案,其中正确的是( )
A.甲同学:在醋酸钠溶液中滴加2滴酚酞试剂,加热后红色加深,说明盐类水解是吸热的。
B.乙同学:在盐酸中加入氨水,混合液温度上升,说明盐类水解是吸热的。
C.丙同学:将硝酸铵晶体溶于水,水温降低,说明盐类水解是吸热的。
D.丁同学:在氨水加入氯化铵固体,溶液的pH变小,说明盐类水解是吸热的。
⑷ 为探究纯碱溶液呈碱性是由CO32-引起的,请你设计一个简单的实验方案。
参考答案:(8分)(每空2分)
⑴ 把小块pH试纸放在表面皿(或
本题解析:(2)Na2CO3溶液中由于CO32-水解,CO32-+H2O HCO3-+OH-,导致c(Na+)>2 c(CO32-)。故可以加KOH,抑制其水解,符合题意。但加盐酸将发生:CO32-+H+=HCO3-,破坏CO32-,不符合题意;同样,加水稀释会促进其水解,不符合题意;加适量的NaOH,虽然能抑制其水解,但同时增加了Na+,不会满足题意 HCO3-+OH-,导致c(Na+)>2 c(CO32-)。故可以加KOH,抑制其水解,符合题意。但加盐酸将发生:CO32-+H+=HCO3-,破坏CO32-,不符合题意;同样,加水稀释会促进其水解,不符合题意;加适量的NaOH,虽然能抑制其水解,但同时增加了Na+,不会满足题意
(3)B:本质是发生了中和反应,有中和热的放出,导致温度升高
C:硝酸铵晶体溶于水,其溶解过程是吸热过程,导致水温降低
D:氨水加入氯化铵固体,是由于氨根离子的增多,抑制了氨水的电离,导致碱性减弱
本题难度:困难
|