微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 自来水可用氯气消毒,某学生用这种自来水去配制下列物质溶液,不会产生明显的试剂变质问题的是[???? ]
A.AgNO3
B.FeCl2
C.Na2SO3
D.AlCl3
参考答案:D
本题解析:
本题难度:简单
2、选择题 下列关于中学化学中的“水”对应正确的是 [???? ]
A.蒸馏水-H2O
B.氯水-Cl2、H2O、HClO、H+、Cl-、ClO-、 OH-(少量)
C.王水-浓盐酸与浓硝酸的物质的量之比为 1:3
D.硬水-含Mg2+、Ca2+的水,软水-不含Mg2+、Ca2+的水
参考答案:AB
本题解析:
本题难度:简单
3、简答题 (14分)
研究小组用下图装置制取Cl2,证明产生的气体中含有HCl。

(1)仪器A的名称为??????;A中反应的离子方程式为??????。
(2)甲同学将A中产生的气体通入下列溶液:
实验序号
| 试剂
| 现象
|
a
| 紫色石蕊溶液
| ????????????????
|
b
| AgNO3溶液
| 出现白色沉淀
①实验a中的现象为????????。
②不能证明产生的气体中含有HCl的实验是???????(填字母序号)。
(3)已知将HCl气体通入饱和食盐水中有白色固体析出。乙同学将A中产生的气体通入饱和食盐水中,有白色固体析出,但该实验不能证明气体中含有HCl,结合化学用语解释其原因:??????。
(4)已知:2S2O32- + I2 ="==" S4O62- + 2I-。丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl。
I.测定X中溶解的Cl2。取25.00 mL溶液X,加入过量KI溶液,然后用0.04 mol?L-1 Na2S2O3溶液滴定生成的I2,达滴定终点时消耗Na2S2O3溶液V mL。
II.测定X中Cl元素总量。另取25.00 mL溶液X,选用适当的还原剂将溶解的Cl2全部还原为Cl-,再用0.10 mol?L-1 AgNO3溶液滴定所得溶液中的Cl-。
X中的HClO不会影响I的测定结果,原因是???????。
由I、II 中实验数据可证明A中产生的气体中含有HCl,则II中消耗0.10 mol?L-1 AgNO3溶液的体积应大于???????mL(用含V的代数式表示)。
参考答案:(14分)
(1)圆底烧瓶(1分)? 4H++2Cl-
本题解析:
试题分析:(1)仪器A的名称为圆底烧瓶;A是二氧化锰与浓盐酸制取氯气的反应,离子方程式为4H++2Cl-+MnO2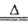 2H2O + Cl2↑+Mn2+ 2H2O + Cl2↑+Mn2+
(2)①氯气溶于水生成氯化氢和次氯酸,溶液呈酸性,所以石蕊试液变红;次氯酸具有漂白性,随后溶液红色褪去;
②ab都不能证明产生的气体中含有HC
本题难度:一般
4、选择题 下列说法不正确的是(????)
A.浓硝酸与足量铜片反应时,先生成红棕色气体,后生成无色气体
B.浓硫酸具有强氧化性,常温下可将铁、铝的单质氧化
C.饱和氯水既有酸性又有漂白性,加入NaHCO?后漂白性减弱
D.浓盐酸与足量二氧化锰反应后,盐酸有剩余
参考答案:C
本题解析:
试题分析:A.浓硝酸与足量铜片反应时,开始硝酸是浓度大的,浓硝酸和铜发生反应产生硝酸铜、二氧化氮和水;随着反应的进行。硝酸变稀,这时是铜与稀硝酸发生反应产生硝酸铜、一氧化氮和水。二氧化氮是红棕色的气体,一氧化氮是无色气体。所以先生成红棕色气体,后生成无色气体。正确。B.浓硫酸具有强氧化性,但常温下遇到铁、铝的单质因氧化产生致密的氧化物保护膜。产生钝化现象。正确。C.氯气溶于水得到氯水。氯气和水发生反应产生盐酸和次氯酸。这是个可能反应。含有氯气、次氯酸、盐酸。氯气、次氯酸有漂白性,盐酸有酸性,酸性比
本题难度:一般
5、填空题 (10分)新制氯水中含有Cl2、H2O、HClO、H+、Cl-等粒子,根据下列性质选择恰当的粒子进行填空。
(1)使新制氯水呈现浅黄绿色的物质是??????????????;
(2)能起杀菌消毒作用,光照易分解的弱酸是???????????;
(3)能与硝酸银溶液作用生成白色沉淀的离子是?????????。
(4)取少量新制氯水于试管中,加入FeCl2溶液,发现很快变黄,起作用的成分是Cl2,说明氯气具有?????????性。写出该反应的离子方程式????????????????????。
参考答案:(1)Cl2(2)HClO?(3)Cl- ?(4)氧化?2F
本题解析:(1)氯气为黄绿色气体,在水中溶解度较小,从而使新制氯水呈现浅黄绿色;
(4)2FeCl2+Cl2=2FeCl3,Cl2中氯的化合价由0价降低到-1价,被还原,做氧化剂;
本题难度:一般
|