微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 镁、铝、铁及其化合物在生产和生活中有广泛的应用。
(1)镁铝合金用在飞机制造业,现有3.90克镁铝合金溶于足量的2mol/L稀硫酸中生成0.2mol氢气,计算并确定镁铝合金中物质的量n(Mg): n(Al)=????????。
(2)硫铁矿的主要成分为FeS2(假设杂质只含SiO2)是生产硫酸的原料。取某硫铁矿10g在足量的空气中煅烧(4FeS2+11O2→2Fe2O3+8SO2),充分反应后冷却,称得固体质量为7.4g(杂质SiO2不反应)。该硫铁矿中FeS2的质量分数为??????????????。
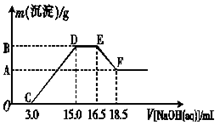
(3)现有一定量的铁粉和铝粉组成的混合物跟100 mL稀硝酸充分反应,反应过程中无任何气体放出,往反应后的澄清溶液中逐渐加入4.00 mol・L-1的NaOH溶液,加入NaOH溶液的体积与产生沉淀的质量的关系如图所示(必要时可加热,忽略气体在水中的溶解):纵坐标中A点的数值是???????????????。
(4)炼铁厂生产的生铁常用于炼钢。取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,得到CO2气体224mL(标准状况下)。
①计算此钢样粉末中铁和碳的物质的量之比为????????????????(最简单的整数比)。
②再取三份不同质量的上述钢样粉末分别加到100mL相同浓度的稀H2SO4中,充分反应后,测得的实验数据如下表所示:
实验序号
| Ⅰ
| Ⅱ
| Ⅲ
|
加入钢样粉末的质量(g)
| 2.812
| 5.624
| 8.436
|
生成气体的体积(L)(标准状况)
| 1.120
| 2.240
| 2.800
?
则该硫酸溶液的物质的量浓度为??????????????????。
③若在上述实验Ⅱ中继续加入m克钢样粉末,计算反应结束后剩余的固体质量为???g (保留3位小数)
2、选择题 下列说法正确的是( )
A.2mol的盐酸
B.0.1mol氢
C.0.3molHCl
D.4mol的氧元素
3、选择题 在体积aL的密闭容器中,放入2 L A气体和1 L B气体,在一定条件下发生反应:3A(g)+B(g) nC(g)+2D(g),反应达平衡后,A的浓度减少到原来的1/2,混合气体的平均相对分子质量增大了1/8倍,则反应式中的n值为(???) nC(g)+2D(g),反应达平衡后,A的浓度减少到原来的1/2,混合气体的平均相对分子质量增大了1/8倍,则反应式中的n值为(???)
A.1
B.2
C.3
D.4
4、选择题 设NA表示阿伏加德罗常数的数值,下列有关说法中正确的是(??)。
A.15 g CH3+含电子数为10 NA
B.78 g Na2O2发生氧化还原反应,转移电子数一定是NA
C.一定条件下,向密闭容器中充入1 mol N2与3 mol H2,发生化学反应转移电子数为6 NA
D.22.4 L(标况下)氯气与足量的铁、铜在一定条件下发生反应,转移电子数均为2 NA
5、选择题 将30mL0.5mol/LNaOH溶液加水稀释到1000mL,稀释后NaOH的物质的量浓度为( )
A.0.3mol/L
B.0.015mol/L
C.0.05?mol/L
D.0.04mol/L
|