微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下,可用铁或铝制容器盛装冷的浓硫酸,是因为其发生了钝化,这表现浓硫酸的(?????)
A.吸水性
B.脱水性
C.强氧化性
D.酸性
参考答案:C
本题解析:
试题分析:浓硫酸具有强氧化性,常温下能使铁、铝等金属钝化,生成氧化膜,阻止反应的继续进行:
4Al+12HNO3(浓)=2Al2O3+12NO2↑+6H2O
4Fe+12HNO3(浓)=2Fe2O3+12NO2↑+6H2O
点评:本题考查浓硫酸的性质,弄清钝化的原理是解答本题的关键。
本题难度:一般
2、填空题 能证明SO2中混有CO2的方法是
A.通过品红溶液
B.通过澄清石灰水
C.先通过高锰酸钾溶液,再通过澄清石灰水
D.先通过澄清石灰水, 再通过高锰酸钾溶液
参考答案:C
本题解析:因SO2也能使澄清石灰水变浑浊,故先将混合气体通过高锰酸钾溶液,除去SO2(两者发生氧化还原反应),再通过澄清石灰水(与CO2反应,生成白色沉淀)来验证SO2中混有CO2;
本题难度:一般
3、选择题 硫酸和硝酸的混合溶液20mL,其中含有硫酸的浓度为2mol/L,含硝酸的浓度是1mol/L,现向其中加入0.96g铜粉,充分反应后(假设只生成NO气体),最多可收集到标准状况下的气体的体积为(???)
A.89.6mL
B.112mL
C.168mL
D.224mL
参考答案:D
本题解析:因为只要溶液显酸性,硝酸盐就具有强氧化性,所以本题应该通过离子方程式进行应该的计算。溶液中氢离子的物质的量是0.02L×(2mol/L×2+1mol/L)=0.1mol,0.96g铜的物质的量是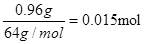 。根据反应式可知
。根据反应式可知
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3??? 8???2????
本题难度:一般
4、填空题 在下列反应中:?
2FeO+4H2SO4(浓)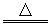 Fe2(SO4)3+SO2↑+4H2O?
Fe2(SO4)3+SO2↑+4H2O?
H2SO4表现出的性质是____________,FeO表现出的性质是____________;该反应的氧化产物和还原产物的物质的量之比是____________。
参考答案:氧化性和酸性 还原性和碱性 1∶1
本题解析:H2SO4变为盐〔Fe2(SO4)3〕和水,表现了H2S+6O4的酸性;H2SO4变为S+4O2,表现了H2SO4的氧化性。FeO变为盐〔Fe2(SO4)3〕和水,表现了FeO的碱性;F+2eO变为F+3e2(SO4)3,表现FeO的还原性。氧化产物是Fe2(SO4)3,还原产物是SO2,二者物质的量之比为其化学计量数之比即1∶1。
本题难度:简单
5、填空题 (15分)以黄铁矿为原料生产硫酸的工艺流程图如下:
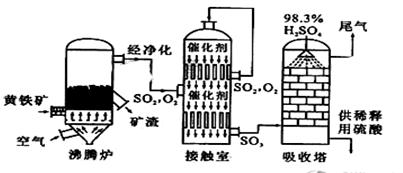
(1)写出燃烧黄铁矿的化学方程式????????????????????????????????。
当有6mol SO2生成时,转移电子???????mol。
(2)进入接触室的气体中含标准状态下1120m3SO2气体,达平衡后放出热量为4.728×106kJ,此时SO2转化率为96%。该反应的热化学方程式为??????????????。
(3)依据工艺流程图判断下列说法正确的是(选填序号字母)????????。
a.为使黄铁矿充分燃烧,需将其粉碎????????????
b.过量空气能提高SO2的转化率
c.使用催化剂能提高SO2的反应速率和转化率
d.沸腾炉排出的矿渣可供炼铁???????????????
e.吸收塔用水作吸收剂
(4)某硫酸厂在进行黄铁矿成分测定时,取0.1000 g样品充分灼烧,生成的SO2气体与足量Fe2(SO4)3溶液完全反应后,再用0.02000 mol・L-1的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00mL。
已知:SO2+2Fe3++2H2O=SO42-+2Fe2++4H+
Cr2O72-+6Fe2++14H+ =2Cr3++6Fe3++7H2O
则样品中FeS2的质量分数是多少?(假设杂质不参加反应)
(5)该生产过程中产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。能用于测定硫酸尾气中SO2含量的是????????。(填字母)
A.NaOH溶液、酚酞试液
B.KMnO4溶液、稀H2SO4
C.碘水、淀粉溶液
D.氨水、酚酞
参考答案:(1)4FeS2?+ 11O2  本题解析:(1)黄铁矿燃烧生成SO2和氧化铁,方程式为4FeS2?+ 11O2
本题解析:(1)黄铁矿燃烧生成SO2和氧化铁,方程式为4FeS2?+ 11O2 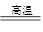 ?2Fe2O3+8SO2 。反应中氧气是氧化剂,转移电子是44,所以当有6mol SO2生成时,转移电子44mol÷8×6=33mol。
?2Fe2O3+8SO2 。反应中氧气是氧化剂,转移电子是44,所以当有6mol SO2生成时,转移电子44mol÷8×6=33mol。
(2)标准状态下1120m3SO2气体是50000mol,所以反应中消耗的SO2是50000mol
本题难度:一般