微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (12分)用含少量铁的氧化铜制取氯化铜晶体(CuCl2・xH2O)。有如下操作:
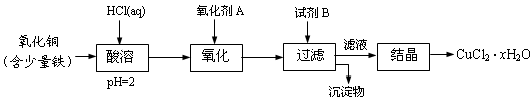
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,而此时Cu2+却几乎不水解。
(1)氧化剂A可选用_______(填编号,下同)
① Cl2???????????? ② KMnO4??????? ③ HNO3???????? ④ H2O2
(2)要得到较纯的产品,试剂B可选用_______???
① NaOH??????????? ② FeO ???????????? ③ CuO????????? ④Cu2(OH)2CO3
(3)试剂B的作用是______??????
① 提高溶液的pH ② 降低溶液的pH ?? ③ 使Fe3+完全沉淀?? ④ 使Cu2+完全沉淀
(4)从滤液经过结晶得到氯化铜晶体的方法是_________(按实验先后顺序选填编号)
① 过滤???????? ② 蒸发浓缩???????? ③ 蒸发至干???????? ④ 冷却
(5)为了测定制得的氯化铜晶体(CuCl2・xH2O)中x值,某兴趣小组设计了两种实验方案:
方案一:称取m g晶体灼烧至质量不再减轻为止,冷却、称量所得无水CuCl2的质量为n g。
方案二:称取m g晶体、加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再减轻为止、冷却、称量所得固体的质量为n g。
试评价上述两种实验方案,其中正确的方案是______,据此计算得x = _________(用含m、n的代数式表示)。
参考答案:(12分)(1) ①④(2分)
(2) ③④(2分)<
本题解析:
试题分析:(1)四种试剂都具有强氧化性,为的是制取氯化铜晶体,选用的氧化剂反应后不能生成其它杂质离子,因此选用① Cl2 ④ H2O2。(2)试剂B与氧化剂A选择条件是相似的,因此选用③ CuO④Cu2(OH)2CO3。(3)选择的试剂B,通过与酸的反应生成Cu2+且提高溶液的pH。因在pH为4~5时,Fe3+几乎完全水解而沉淀,而此时Cu2+却几乎不水解。所以促使了Fe3+完全沉淀。(4)氯化铜晶体的生成,对滤液先加热蒸发使水份减少溶液浓缩,再冷却结晶,过滤就得到了氯化铜晶体。(5)氯化铜晶体灼烧的温度足以分解氯化铜,氯化铜经过灼烧是不能以氯化铜的形式存在的,会分解为CuO,CuCl2+2H2O Cu(OH)2+2HCl Cu(OH)2
Cu(OH)2+2HCl Cu(OH)2 CuO + H20,固体不可能为纯净的CuCl2,因此第一种方法不正确。第二方案中,最终生成的是CuO,根据铜原子守恒可得:
CuO + H20,固体不可能为纯净的CuCl2,因此第一种方法不正确。第二方案中,最终生成的是CuO,根据铜原子守恒可得:
CuCl2?xH2O → CuO
135+18x ??????80
m ????????????n
(135+18x)/m = 80/n
x=(80m-135n)/18n
点评:解答本题找准考点是关键,考查了盐类水解,注意方案一中最终的固体不可能为纯净的CuCl2。
本题难度:一般
2、填空题 用Na2CO3沉淀CaCl2溶液中的钙离子,如何检验Ca2+已经沉淀完全______.
参考答案:CaCl2和Na2CO3反应生成碳酸钙和氯化钠,Na2CO3
本题解析:
本题难度:一般
3、实验题 某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示的装置进行有关实验。请回答:
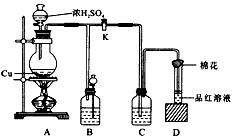
(1)装置A中发生的化学方程式为______________________。
(2)装置D中试管口放置的棉花中应浸入一种液体,这种液体是____,其作用是____。
(3)装置B的作用是储存多余的气体。当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A 处仍有气体产生,此时B中现象是_______________。 B中应放置的液体是_____。(填字母)。
a.水
b.酸性KMnO4溶液?
c.浓溴水
d.饱和NaHSO3溶液
(4)实验中,取一定质量的铜片与一定体积18 mol/L的浓硫酸放在圆底烧瓶中共热,直到反应完毕。发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是__________________。
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是____________(填字母)
a.铁粉
b.BaCl2溶液
c.银粉
d.Na2CO3溶液
参考答案:(1)![]() 本题解析:
本题解析:
本题难度:一般
4、实验题 甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)。

|
实验操作和现象

⑴A中反应的化学方程式是_______________。
⑵C中白色沉淀是__________,该沉淀的生成表明SO2具有____________性。
⑶C中液面上方生成浅棕色气体的化学方程式是____________________________。
⑷分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应。
①为证实各自的观点,在原实验基础上:甲在原有操作之前增加一步操作,该操作是______________;乙在A、B间增加洗气瓶D,D中盛放的试剂是______________。
②进行实验,B中现象
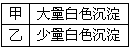
检验白色沉淀,发现均不溶于稀盐酸。结合离子方程式解释实验现象异同的原因:______________。
⑸合并⑷中两同学的方案进行实验。B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是____________________________。
参考答案:⑴Cu+2H2SO4![]() 本题解析:
本题解析:
本题难度:困难
5、选择题 下列实验方法或结论中,不正确的是( )
A.用焰色反应能鉴别NaCl、KCl和Na2SO4三种物质
B.向某溶液中加入KSCN溶液变红色,说明该溶液中含有Fe3+
C.将溴水倒入分液漏斗,加适量四氯化碳,振荡后静置,可将溴萃取到四氯化碳中
D.某无色溶液中加入稀盐酸,无明显现象,再加BaCl2溶液,有白色沉淀生成,则该溶液中一定含有SO42-
参考答案:A.NaCl、Na2SO4焰色反应都呈黄色,焰色反应不能鉴别
本题解析:
本题难度:简单