��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� 25��ʱ����ͬ���ʵ���Ũ�ȵ�������Һ��
����ˮ�ĵ���̶Ȱ��ɴ�С˳�����е�һ����
A����>��>��>��
B����>��>��>��
C����>��>��>��
D����>��>��>��
�ο��𰸣�D
���������
����������������ˮ�ĵ��룬��ˮ����δٽ�ˮ�ĵ��룬ǿ��ǿ���ζ�ˮ�ĵ�����Ӱ�죬����ˮ��������еĵ���̶��������Ũ��Խ��ˮ�ĵ������Ƴ̶�Խ������ͬŨ�ȵ�NaOH��H2SO4��Һ�У�ˮ�������еĵ���̶���С�����ˮ�ĵ���̶Ȱ��ɴ�С˳�����е��Ǣ�>��>��>�ۣ�ѡD��
���㣺����Ӱ��ˮ�ĵ���ƽ������ء�
�����Ѷȣ�һ��
2��ѡ���� �������ʵĵ��뷽��ʽ��ȷ���ǣ� ? ��
A��H2CO3?2H++CO32-
B��HClO�TH++ClO-
C��NaHCO3?Na++HCO3-
D��Ba��OH��2�TBa2++2OH-
�ο��𰸣�D
���������
�����Ѷȣ���
3�������� 25��Cʱ�������ΪVa��pH=a��ijһԪǿ�������ΪVb��pH="b" ��ijһԪǿ���ϣ�ǡ���кͣ�����֪Va��Vb��a=0.5b,����д���пհף�
��1��aֵ�ɷ����3 ����ɡ�������������
��2��aֵ�ɷ����5 ����ɡ�������������
��3��a��ȡֵ��Χ��
�ο��𰸣���1������a=3����b=6������Һ�����ԣ������ⲻ��
�������������pH���йؼ��㡣
��1�����a=3�������a��0.5b��֪��b=6�������ڳ����¼���Һ��pHһ���Ǵ���7�ģ���˼����Dz��ܳ����ġ�
��2�����a=5�������a��0.5b��֪��b=10����ʱc(H+)��10��5 mol/L��c(OH-)=10��4 mol/L,
Va/Vb= c(OH-)/c(H+)��1����������.��˼����Dz��ܳ����ġ�
��3������Va/Vb= c(OH-)/c(H+)��֪��Va/Vb= 10��a+b-14��<1 ���ʣ�a+b��14��<0������a=0.5b,���3a<14��a<14/3��pH=b=2a>7������3.5<a<14/3��
�����Ѷȣ�����
4��ѡ���� ��֤��һƿ��ɫҺ���Ǵ�ˮ���ɿ���ʵ�鷽���ǣ�
A�������pH=7
B�����ʱ�õ�H2��O2�������Ϊ2��1
C��������������
D��1.01�� 105Paʱ�е�Ϊ100��
�ο��𰸣�D
���������
���������A��pH=7��Һ��Ϊ���ԣ���һ���Ǵ�ˮ������B���������������Һ��ϡ������Һ�ȶ���õ�H2��O2�������Ϊ2��1������C�����Ʒ�Ӧ����������Һ�廹�������ᣬ����D��������ķе��ǹ̶��ģ�ֻ�д�ˮ��1.01�� 105Paʱ�е�Ϊ100�棬��ȷ����ѡD��
���㣺����ʵ�鷽��������
�����Ѷȣ�һ��
5������� (14��)
��1��25 ��ʱ����pH=11��NaOH��Һ��pH=4��������Һ��ϣ������û����ҺpH=9����NaOH��Һ��������Һ�������Ϊ
��֪25 ��ʱ��0.1 L 0.1 mol��L-1��NaA��Һ��pH=10,��Һ�и����ӵ����ʵ���Ũ���ɴ�С��˳��Ϊ ��
��2������100 ��ʱ��KW=10-12����100 ��ʱpH=11��Ba(OH)2��Һ��pH=2�����ᰴ�����1:9��ϳ�ַ�Ӧ��pH= �������¶���10�����pH=a��ijǿ����Һ��1���pH=b��ijǿ����Һ��Ϻ���Һ�����ԣ�����֮ǰ,a��b֮��Ӧ����Ĺ�ϵΪ  ��
��
��3��ij�¶��µ�ˮ��Һ�У�c��H+��=10x mol/L��c��OH-��=10y mol/L��x��y�Ĺ�ϵ��ͼ��ʾ��
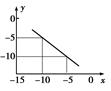
���¶���ˮ�����ӻ�Ϊ �����¶����Ȼ�����Һ��pHΪ
���¶���0.01 mol/L NaOH��Һ��pHΪ ��
�ο��𰸣�(14��)ÿ��2��
��1���������Ϊ
�����������
�����Ѷȣ�һ��