微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 关于小苏打水溶液的表述正确的是
A.c(Na+)+ c(H+)=c(HCO3―)+ c(CO32―)+ c(OH―)
B.c (Na+)= c(HCO3―)+ c(CO32―)+ c(H2CO3)
C.HCO3―的电离程度大于HCO3―的水解程度
D.存在的电离有:NaHCO3=Na++HCO3―;HCO3― H++CO32―
H++CO32―
参考答案:B
本题解析:
试题分析:A、不符合电荷守恒,应该是c(Na+)+ c(H+)=c(HCO3―)+ 2c(CO32―)+ c(OH―),A不正确;B、符合物料守恒,正确;C、碳酸氢钠溶液中HCO3―的电离程度小于HCO3―的水解程度,溶液显碱性,C不正确;D、溶液中还存在水的电离平衡,D不正确,答案选B。
本题难度:一般
2、选择题 下列化肥:①(NH4)2SO4? ②氨水? ③过磷酸钙? ④K2CO3? ⑤KCl ⑥尿素,其中能混合使用的是
A.①④⑤
B.③⑤⑥
C.②③⑤
D.③④⑥
参考答案:B
本题解析:
由上述化肥的性质可知,①③呈酸性,⑤⑥呈中性,②④呈碱性,根据呈酸性的肥料不能和呈碱性的肥料混合使用的原则,只有B选项合理。
本题难度:一般
3、选择题 下列叙述正确的是
A.将一定体积醋酸溶液加水至原来体积的m倍,则pH增大m
B.250C, pH=13的Ba(OH)2溶液和pH=1的盐酸中均存在: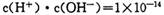
C 250C, pH=8的NaOH溶液和pH=8的氨水中,由水电离出的c (0H_)不相等
D.在NaHCO3溶液中:
参考答案:B
本题解析:本题考查水溶液的离子平衡的有关知识。醋酸是弱酸,在加水稀释过程中,继续电离,产生更多的氢离子,则pH增大小于lgm倍,A错;水的离子常数只与温度有关,与溶液中的氢离子或氢氧根离子浓度大小无关,温度不变,水的离子积就不变,250C时为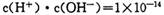 ,B正确;在水中加碱抑制水的电离,pH=8的NaOH溶液和pH=8的氨水中,OH
,B正确;在水中加碱抑制水的电离,pH=8的NaOH溶液和pH=8的氨水中,OH
本题难度:一般
4、填空题 (8分)已知:A酸的溶液pH=a,B碱的溶液pH=b。
(1)若A为盐酸,B为氢氧化钡,且a+b=14,两者等体积混合,溶液的pH=________。酸碱按体积比为1 ∶10混合后溶液显中性,则a+b=________。
(2)若A为醋酸,B为氢氧化钠,且a=4,b=12,那么A溶液中水电离出的氢离子浓度为________mol・L-1,B溶液中水电离出的氢离子浓度为________mol・L-1。
(3)若A为醋酸,B为氢氧化钠,且a+b=14,用体积为VA的醋酸和体积为VB的氢氧化钠溶液混合后,溶液显中性,则其体积关系为VA________VB(填“>”、“<”或“=”,下同),混合后溶液中的离子浓度关系为c(Na+)________
c(CH3COO-)。
(4)若A的化学式为HR,B的化学式为MOH,且a+b=14,两者等体积混合后溶液显碱性。则混合溶液中必定有一种离子能发生水解,该水解反应的离子方程式为________________________________________________________________________
________________________________________________________________________。
参考答案:(1)7 13 (2)10-10 10-12 (3)<
本题解析:根据题意,A酸中c(H+)=10-a,B碱中c(OH-)=10b-14,酸碱发生中和反应呈中性时,n(H+)=n(OH-),有VA×10-a=VB×10b-14,VA∶VB=10a+b-14,若a+b=14,则VA=VB,若a+b>14,则VA>VB,若a+b<14,则VA<VB。a+b=14的弱酸和强碱混合呈中性,则酸需要体积小,a+b=14的一元酸和一元碱混合呈碱性,则碱是弱碱。
本题难度:一般
5、选择题 下列叙述正确的是
A.0.1mol・L-1氨水中,c(OH-)=c(NH4+)
B.在0.1mol・L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+)
C.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-)??
D.0.1mol・L-1某二元弱酸强碱盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A)
参考答案:B
本题解析:
试题分析:A不正确,因为水还能电离出OH-,所以c(OH-)>c(NH4+);B正确,因为满足质子守恒;C不正确,因为根据电荷守恒c(Na+)+c(H+)=c(X-)+c(OH-),所以C不正确;D不正确,不符合物料守恒,应该是c(Na+)=c(A2-)+c(HA-)+c(H2A),答案选B。
点评:比较溶液中离子浓度时,需要遵循几个守恒关系式,即物料守恒、电荷守恒和质子守恒等。另外还需要考虑到溶液中的平衡状
本题难度:一般