微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某溶液中加入铝片有氢气产生,则该溶液中一定能大量共存的离子组是(????)
A.Cl― NO3― Ba2+ Fe3+
B.SO42― S2― Al3+ Mg2+
C.Na+ K+ SO42― Cl―
D.NH4+ Ba2+ Cl― HCO3―
参考答案:C
本题解析:略
本题难度:简单
2、选择题 在天平两边各放一只盛有相同浓度、相同体积的足量盐酸溶液的烧杯,调节天平到平衡,在左边烧杯中放入3.6的铝粉,为使天平最终保持平衡,右边烧杯中应放入镁粉的量是?????????????(??)
A.3.49g
B.3.60g
C.3.81g
D.3.92g
参考答案:A
本题解析:略
本题难度:简单
3、选择题 金属铝既可与强酸溶液反应,又可与强碱溶液反应.当金属铝和适量的NaOH溶液恰好完全反应时,下列说法合理的是
A.该反应中的氧化剂有两种,而还原产物只有一种
B.1mol铝完全反应生成33.6L氢气
C.所得溶液蒸干并灼烧会生成氧化铝
D.54?g铝完全反应,水得到的电子数为6NA
参考答案:D
本题解析:分析:A、铝碱溶液反应的本质,是铝与水反应生成氢氧化铝与氢气,氢氧化铝再与氢氧化钠反应,生成偏铝酸盐;
B、氢气所处的状态不一定是标准状况;
C、偏铝酸钠水解呈碱性,生成的氢氧化钠与氢氧化铝反应生成偏铝酸钠;
D、根据n=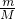 计算铝的质量,反应中水是氧化剂,Al是还原剂,Al元素化合价由0价升高为+3价,据此计算转移电子数目.
计算铝的质量,反应中水是氧化剂,Al是还原剂,Al元素化合价由0价升高为+3价,据此计算转移电子数目.
解答:A、铝碱溶液反应的本质,是铝与水反应生成氢氧化铝与氢气,氢氧化铝再与氢氧化钠反应,生成偏铝酸盐,反应中Al是还原剂,水是氧化剂,还原产物是氢气,氧化剂有1种,还原产物有1种,故A错误;
B、1molAl反应转移3mol电子,生成1.5mol氢气,若氢气为标准化状况,体积为33.6L,但氢气所处的状态不一定是标准状况,故B错误;
C、偏铝酸钠水解呈碱性,生成的氢氧化钠与氢氧化铝反应生成偏铝酸钠,故蒸干偏铝酸钠溶液,获得的固体为偏铝酸钠,故C错误;
D、54g铝的物质的量为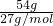 =2mol,反应中水是氧化剂,Al是还原剂,Al元素化合价由0价升高为+3价,故Z转移电子数目为2mol×3×NAmol-1=6NA,故D正确;
=2mol,反应中水是氧化剂,Al是还原剂,Al元素化合价由0价升高为+3价,故Z转移电子数目为2mol×3×NAmol-1=6NA,故D正确;
故选D.
点评:本题考查铝的性质、盐类水解、氧化还原反应及计算等,难度不大,注意A选项为易错点,理解铝与碱溶液反应的本质.
本题难度:一般
4、选择题 铝已被世界卫生组织确定为食品污染源之一,要求加以控制使用。铝在下列应用中应该加以控制使用的是
①制铝合金②制电线③制炊具④用明矾净水⑤制易拉罐⑥油漆颜料
⑦明矾与苏打制食品膨化剂?⑧用氢氧化铝凝胶制胃舒平药片?⑨包装糖果和小食品
A.⑤⑦⑧⑨
B.①②⑥
C.④⑦⑧
D.③④⑤⑦⑧⑨
参考答案:D
本题解析:可能造成人们摄入铝的应用应该加以控制。
本题难度:一般
5、选择题 下图为A、B两种物质间的转化关系(其中C、D是反应物,部分产物已省略)。

以下判断不正确的是
A.若A是AlCl3,则C既可以是强碱,也可以是弱碱
B.若A是碱性气体,则A和C可能发生氧化还原反应,也可能发生非氧化还原反应
C.上述变化过程中,A可以是酸、碱、盐,也可以是单质或氧化物
D.若A→B是氧化还原反应,则C、D在上述转化过程中一定有一种为氧化剂,另一种为还原剂
参考答案:D
本题解析:
试题分析:A、AlCl3既可以与强碱反应,也可以与弱碱反应,如NH3?H2O、NaOH,都能生成Al(OH)3,正确;B、若A是碱性气体,为NH3,可以与酸生成铵盐,为非氧化还原反应,也可以与O2、Cl2等发生氧化还原反应,正确;C、A可以是酸、碱、盐,通过复分解反应相互转化,也可以是单质或氧化物,通过氧化还原反应相互转化,正确;D、C或D可能既不作氧化剂也不作还原剂,例如:Na2O2与CO2或H2O的反应,错误。
本题难度:一般