微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 某课题组研究以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3・6H2O)的工艺,其设计的流程如下:

回答下列问题:
(1)已知在焙烧硫铁矿石过程中铁元素转化成了Fe3O4,则该反应的化学方程式?????????????????;
(2)“酸溶”中反应的离子方程式为?????????????????????????????????????;
(3)“过滤”后滤液中金属阳离子有???????????????????;
(4)“氧化”中使用的氧化剂最好是????????????????????;
(5)该工艺流程中产生的SO2会污染空气并形成酸雨,下列物质:①BaCl2②品红③石灰乳 ④O2,用于吸收SO2最好的是??????????????。
2、选择题 要检验久置的FeSO4溶液是否含有Fe2(SO4)3,应选用的试剂是
A.NH4SCN溶液
B.KI溶液
C.氨水
D.Fe粉
3、选择题 红珊瑚栖息于200~2000米的海域,产于台湾海峡、南中国海,它与琥珀、珍珠被统称为有机宝石.在中国,珊瑚是吉祥富有的象征,一直用来制做珍贵的工艺品.红珊瑚是无数珊瑚虫分泌的石灰质大量堆积形成的干支状物,其红色是因为在海底长期积淀某种元素,该元素是( )
A.Na
B.Fe
C.Si
D.Cu
4、填空题 以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等。实验室模拟工业以硫酸渣制备铁红(Fe2O3),过程如下:
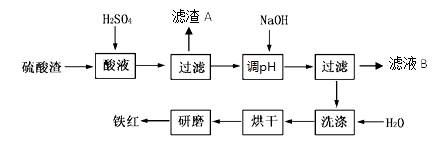
(1)硫酸渣的成分中属于两性氧化物的是???????,写出酸溶过程Fe2O3与稀硫酸反应的离子反应方程式????????????????;
(2)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是???????????(部分阳离子以氢氧化物形式沉淀时溶液的pH见下表)
沉淀物
| Fe(OH)3
| Al(OH)3
| Fe(OH)2
| Mg(OH)2
|
开始沉淀
| 2.7
| 3.8
| 7.5
| 9.4
|
完全沉淀
| 3.2
| 5.2
| 9.7
| 12.4
?
(3)滤渣A的主要成分为??????,滤液B可以回收的物质有____________;
(4)简述洗涤过程的实验操作????????????????????????????????????;
(5)已知硫酸渣质量为w kg,假设铁红制备过程中,铁元素损耗25%,最终得到铁红的质量为m kg,则原来硫酸渣中铁元素质量分数为????????(用最简分数表达式表示)。
5、填空题 (一)含铜物质是化学中的重要试剂。例如利用新制氢氧化铜悬浊液验证葡萄糖的还原性。
新制氢氧化铜悬浊液的配制与应用:
(1)实验室制取新制氢氧化铜悬浊液的操作方法:在试管里加入10%的________溶液2mL,滴入2%的_________溶液4~6滴(以上选填“硫酸铜”或“氢氧化钠”),振荡即成。这样操作的目的_______________________________________________。
(2)下列各组物质的溶液仅用新制的氢氧化铜悬浊液(必要时可以加热)不能检验出来的是______。
A.HCOOCH3,C6H5COOH,C6H5CH2OH
B.NaHSO4,BaCl2,Na2CO3,酚酞
C.HCOOH,HCOONa,HCOOCH2CH3
D.葡萄糖,CH2OHCHOHCH2OH
(二)下图是某同学在实验室中制取Cl2的装置图:
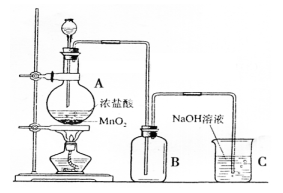
(1)该装置中的错误之处有二,分别是:
①???????????????????????????????????????????????????
②???????????????????????????????????????????????????
(2)试写出装置A和C中发生反应的离子方程式:
A处:?????????????????????????????????????????????????????????;C处:?????????????????????????????????????????????????????????。
|