微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列实验操作正确的是
A.将氢氧化钠固体放在滤纸上称量
B.用10mL量筒量取8.58mL蒸馏水
C.制取SO2时,用Na2SO3与浓硫酸在常温下反应,并用排水集气法收集
D.配制氯化铁溶液时,将氯化铁溶解在较浓盐酸中,再用水稀释到所需浓度
参考答案:D
本题解析:氢氧化钠固体易吸水,且具有腐蚀性,所以应该放在烧杯中称量,A不正确;量筒只能读数到0.1ml,B不正确;SO2易溶于水,应该用向上排气法收集,C不正确;氯化铁易水解,所以选项D上正确的,答案选D。
本题难度:一般
2、选择题 下列有关实验操作、现象或原理均正确的是
选项
| 实验操作
| 实验现象或原理
|
A
| 将海带灼烧,加水浸泡后过滤,向滤液中加入CCl4,振荡后静置
| 液体分层,下层显紫红色
|
B
| 向氢氧化铝胶体中逐滴加入稀盐酸或氢氧化钠稀溶液
| 均先出现沉淀后溶解
|
C
| 将40.0gNaoH固体溶于1.0L蒸馏水中配成溶液
| NaOH的物质的量浓度为1.0mol/L
|
D
| 向BaSO4饱和溶液中加入饱和Na2CO3溶液
| 有白色沉淀产生,说明Ksp(BaSO4)大于Ksp(BaCO3)
参考答案:B
本题解析:
试题分析:A、海带灼烧、加水浸泡后滤液中含有I-,故A错误;B、氢氧化铝胶体中加入电解质会发生胶体的凝聚现象,且氢氧化铝为两性氧化物可溶于强酸、强碱溶液,B正确;C、应为将40.0gNaOH固体溶于水配成1L溶液得到1mol/LNaOH溶液;D、BaSO4溶解度更小,D错误。
本题难度:一般
3、简答题 (1)实验是化学研究的基础,下列有关说法中,正确的是______(填序号字母).
a.可在耐高温的石英坩埚中进行熔化氢氧化钠固体的实验
b.用pH试纸测定溶液的pH时,不需用蒸馏水润湿试纸
c.实验室中不慎将酒精撒在台面上起火,可用湿抹布覆盖灭火
d.实验室取用少量白磷时,可将白磷取出,在空气中用小刀切割
(2)用分液漏斗和烧杯可以装配成一套简易的,能随开随用、随关随停的气体发生装置,如图所示.能用此装置制备的气体有______(填序号字母).
a.用块状大理石与盐酸反应制取CO2
b.用锌粒与稀硫酸反应制取H2
c.用过氧化钠与水反应制取O2
d.用二氧化锰与浓盐酸反应制取Cl2.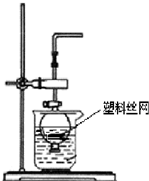
参考答案:(1)a.石英的成分是二氧化硅,二氧化硅是酸性氧化物,能和氢
本题解析:
本题难度:一般
4、选择题 下列叙述正确的是
A.同温同压下,相同体积的物质,它们的物质的量必相等
B.1L一氧化碳气体一定比1L氧气的质量小
C.任何条件下,等物质的量的二氧化碳和一氧化碳所含的分子数必相等
D.等体积、等物质的量浓度的强酸中所含的H+数一定相等
参考答案:C
本题解析:分析:A.阿伏加德罗定律只适用于气体;
B.气体存在的条件位置,不能确定质量大小;
C.根据N=nNA判断;
D.酸能电离出的氢离子个数不一定相同.
解答:A.阿伏加德罗定律只适用于气体,如不是气体,则不能确定物质的量的关系,故A错误;
B.气体存在的条件位置,不能确定质量大小,故B错误;
C.由N=nNA可知任何条件下,等物质的量的二氧化碳和一氧化碳所含的分子数必相等,故C正确;
D.酸能电离出的氢离子个数不一定相同,如硫酸和盐酸,故D错误.
故选C.
点评:本题考查物质的量的相关计算和判断,注意物质存在的状态以及分子构成,题目难度不大.
本题难度:一般
5、实验题 (福建师大附中2008-2009学年高三第一学期第一学段检测,化学,22)(1)用5.0mol/L的NaOH溶液配制2.0mol/L的NaOH溶液时,下图所示的仪器中,肯定不需要的是 (填序号),配制上述溶液还需要的玻璃仪器是 ???????(填仪器名称)。
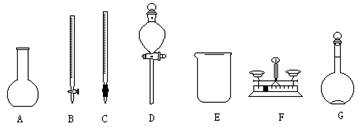
(2)在配制过程中,下列操作将导致实际所配NaOH溶液浓度偏低的是(填编号)??????? _?????? _。
①准确取出的浓NaOH溶液在空气中露置时间过长;②用量器将浓NaOH溶液直接加入容量瓶,缓慢加入蒸馏水至液面最低点恰好和环形刻度线相切;③摇匀后,液面低于刻度线,再加蒸馏水至液面最低点恰好和环形刻度线相切;④用于稀释NaOH溶液的仪器未洗涤。
参考答案:(1)A、B、D、F; 胶头滴管、玻璃棒;(2)①③④。
本题解析:(1)依据用5.0mol/L的NaOH溶液配制2.0mol/L的NaOH溶液步骤为:计算(?mL5.0mol・L-1的硫酸溶液)→量取(量筒或碱式滴定管)→溶解(烧杯、玻璃棒)→冷却到室温→转移(容量瓶)→洗涤→振荡摇匀→定容(胶头滴管)→振荡摇匀,故所选仪器C、E、G,不用的仪器为A、B、D、F,还需要的玻璃仪器是胶头滴管、玻璃棒;(2)①在空气中露置时间过长,NaOH因吸收空气中CO2变质使浓度偏低,②直接加入容量瓶因溶液温度高,相当于溶液体积减小,而使浓度偏高,③摇匀后,液面低于刻度线,再加蒸馏水,相当于溶液体积偏大,而使溶液浓度偏低,④用于稀释NaOH溶液的仪器未洗涤,相当于溶质减少,而使配制溶液浓度偏低。
本题难度:一般
|