��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��������������ͭ�Ļ����ag������2mol/L��������Һ50mLʱ��ǡ����ȫ�ܽ⡣�������������ֻ�����������м��Ȳ���ַ�Ӧ����ȴ��ʣ����������Ϊ
A��0.8g
B��0.8ag
C����a��1.6��g
D����a��0.8��g
�ο��𰸣�C
��������������������ֻ�����������м��Ȳ���ַ�Ӧ����ȴ��ʣ�����Ϊ������ʧȥ����ԭ�ӵ�������SO42�D�����ʵ�����ͬ��2mol/L��005L=0.1mol,����C��ȷ��ѡC��
�����Ѷȣ�һ��
2������� ����8�֣�
0.80gCuSO4��5H2O��Ʒ������ˮ���̵��������ߣ���Ʒ�������¶ȱ仯�����ߣ�����ͼ��ʾ��
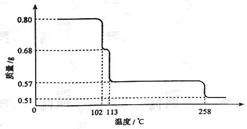
��ش��������⣺
��1����ȷ��200��ʱ�������ʵĻ�ѧʽ______________��Ҫ��д���ƶϹ��̣�
?????????????????????????????????????????????????????????????????????
��2��ȡ270��������Ʒ����570�����յõ�����Ҫ�����Ǻ�ɫ��ĩ��һ�����������壬�÷�Ӧ�Ļ�ѧ����ʽΪ______________���Ѹú�ɫ��ĩ�ܽ���ϡ�����У���Ũ������ȴ���о����������þ���Ļ�ѧʽΪ_________������ڵ�����¶���_____________��
��3������������������ˮ��Ӧ����һ�ֻ�����û������Ũ��Һ��Cu�ڼ���ʱ������Ӧ�Ļ�ѧ����ʽΪ________________��
�ο��𰸣���1��CuSO4��H2O���������̣�����
��2��CuS
�����������
�����Ѷȣ���
3������� ��12�֣�ͨ����ұ��������ͭ�Ǵ�ͭ�������ʽ���������п�������ڵ������������ҵʹ�ã�������е�⾫����
���ھ���ͭʱ��������С���������������ӵ������Ƿ����?? ��??����ǡ���������������������ijɷ���Ҫ��?? ��????��
���ھ���ͭ�Ĺ����У�Cu2+Ũ�����½���c(Fe2+)��c(Zn2+)����?? ��??��������Ҫ��ʱ��ȥ���е�Fe2+��Zn2+����ͬѧ��������г��ӷ���I������ͼ����
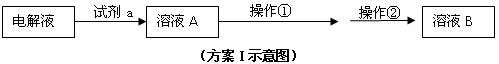
������±����������ݣ��ش��������⣺
��???��
| Fe(OH)2
| Cu(OH)2
| Fe(OH)3
| Zn(OH)2
|
��ʼ����ʱ��pH
| 7.6
| 5.2
| 2.7
| 8.0
|
��ȫ����ʱ��pH
| 9.6
| 6.7
| 3.7
| 11.0
���Լ�a��????? ��??????����Ŀ����????? ��??????��
�ڲ����ٵ���pH��b��b��ȡֵ��Χ��??������?????��
�۵�����ҺA��PHʱ��ѡ��������Щ�Լ�����������������
A��NaOH
B��CuO
C��Cu(OH)2
D��NH3��H2O E��Cu2(OH)2CO3
�ܲ�������??? ��????������I�в��ܹ���ȥ�����ʽ�����������?? ��???��
����ͬѧ�ڲ��Ŀα�ʱ���֣�����ҵԭ���Ȼ���к������Ȼ�����ʹ���ܽ���ˮ���ټ��백ˮ����pH��7-8����ʹFe3+����Fe(OH)3��������ȥ������ͬѧ��Ϊ��ͬѧ�ķ���I��ҲӦ�ý���ҺpH����7-8��
����Ϊ��ͬѧ�Ľ����Ƿ���ȷ��??? ��???����ǡ���������???? ��?????��
�ο��𰸣���12�֣�������ע�⣬ÿ��1�֣�
��1����??????
�����������
�����Ѷȣ���
4��ѡ���� ij������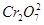 ����ˮ�����������[ ����ˮ�����������[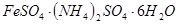 ]��������Ӧ����Ԫ�غ�Ԫ�� ]��������Ӧ����Ԫ�غ�Ԫ�� ��ȫת��Ϊ�������ó��������õ� ��ȫת��Ϊ�������ó��������õ�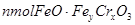 �������Ǵ��������е�ʵ����ģ���������������� �������Ǵ��������е�ʵ����ģ����������������
A��������������淋����ʵ���Ϊ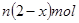
B��������ˮ�е�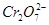 �����ʵ���Ϊ �����ʵ���Ϊ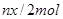
C����Ӧ�з� ��ת�Ƶĵ�����Ϊ ��ת�Ƶĵ�����Ϊ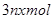
D����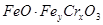 ���� ����
�ο��𰸣�A
�����������
�����Ѷȣ�һ��
5������� �Ȼ������ܲ����ɻ��Ϸ�Ӧ�Ƶã�����д����Ӧ�Ļ�ѧ����ʽ�������ܼ�˵�����ɣ�________________________________________��
�ο��𰸣�2FeCl3+Fe=3FeCl2
�����������
�����Ѷȣ���
|