微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 aF是一种重要的氟盐,主要用作农作物杀虫剂、木材防腐剂等。某课题组设计了以氟硅酸(H2SiF6)等物质为原料制取氟化钠,并得到副产品氯化铵的实验,其工艺流程如下:
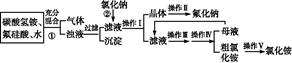
已知:20 ℃时氯化铵的溶解度为37.2 g,氟化钠的溶解度为4 g,Na2SiF6微溶于水。
(1)操作Ⅱ是洗涤、干燥,其目的是 ???????????????????????????????????????,
操作Ⅲ和操作Ⅳ的名称依次是 (填写序号)。
a.过滤??????b.加热蒸发???? c.冷却结晶????? d.洗涤
(2)上述流程中①的化学反应方程式:
H2SiF6+ NH4HCO3 NH4F+? H2SiO3↓+ CO2↑+ ?
NH4F+? H2SiO3↓+ CO2↑+ ?
(3)流程①中NH4HCO3必须过量,其原因是????????????????????????????? 。
(4)若不考虑氟化钠的溶解,7.2 g氟硅酸理论上最多能生产 g氟化钠。
参考答案:(1)除去氟化钠表面的氯化氨杂质 bc
(2)1 6
本题解析:从整个的流程图以及最后得到的产物来看,经①生成的气体是CO2,得到的沉淀是Si元素形成的沉淀。过滤后的滤液中存在F-、N ,加入足量氯化钠后由于氟化钠的溶解度很小,而NaCl、NH4Cl溶解度都较大,所以会生成NaF沉淀;操作Ⅰ是过滤,得到NaF晶体和NH4Cl溶液,操作Ⅱ是洗涤,以除去NaF晶体表面的Cl-、N
,加入足量氯化钠后由于氟化钠的溶解度很小,而NaCl、NH4Cl溶解度都较大,所以会生成NaF沉淀;操作Ⅰ是过滤,得到NaF晶体和NH4Cl溶液,操作Ⅱ是洗涤,以除去NaF晶体表面的Cl-、N 。NH4Cl溶解度较大,需要进行蒸发浓缩、冷却结晶而析出NH4Cl,然后可通过重结晶得到纯净的NH4Cl。在流程①中加入过量NH4HCO3是考虑让H2SiF6完全转化为NH4F,根据原子守恒:m(NaF)=
。NH4Cl溶解度较大,需要进行蒸发浓缩、冷却结晶而析出NH4Cl,然后可通过重结晶得到纯净的NH4Cl。在流程①中加入过量NH4HCO3是考虑让H2SiF6完全转化为NH4F,根据原子守恒:m(NaF)=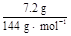 ×6×42 g・ mol-1="12.6" g。
×6×42 g・ mol-1="12.6" g。
本题难度:一般
2、选择题 下列实验设计能够成功的是
?
| 实验目的
| 实验步骤及现象
|
A
| 检验亚硫酸钠试样是否变质
| 
|
B
| 检验某卤代烃是否是氯代烃
| 
|
C
| 证明酸性条件H2O2氧化性比I2强
| 
|
D
| 除去铁屑表面的油污
| 铁屑用热的碳酸钠溶液洗涤,再用蒸馏水冲洗干净
?
参考答案:D
本题解析:
试题分析:A.无法达到实验目的,硝酸可把亚硫酸根离子氧化,错误;B.用硝酸代替硫酸,因为硫酸银也是白色的,错误;C.不应加入HNO3,因为它可以把I-氧化,无法比较H2O2和I2谁的氧化性强,
错误;D.碳酸钠溶液在热的条件下,可以水解为氢氧化钠,油污在氢氧化钠作用下水解,而铁屑和氢氧
化钠不反应。
本题难度:一般
3、选择题 下列除杂质选用的试剂和主要操作都正确的是
?
| 物质
| 杂质
| 试剂
| 主要操作
| A
| CO2
| HCl
| Na2CO3溶液
| 洗气
| B
| NaHCO3溶液
| Na2CO3溶液
| CaCl2溶液
| 过滤
| C
| Cl2
| HCl
| 饱和NaCl溶液
| 洗气
| D
| NaCl溶液
| Na2SO4溶液
| 过量BaCl2溶液
| 过滤
参考答案:C
本题解析:
试题分析:A不正确,应该用饱和碳酸氢钠溶液;B不正确,应该是通入CO2气体;D不正确,应该是适量的氯化钡溶液,答案选C。
点评:把物质中混有的杂质除去而获得纯净物叫提纯,将相互混在一起的不同物质彼此分开而得到相应组分的各纯净物叫分离。在解答物质分离提纯试题时,选择试剂和实验操作方法应遵循三个原则: 1.不能引入新的杂质(水除外),即分离提纯后的物质应是纯净物(或纯净的溶液),不能有其他物质混入其中;2.分离提纯后的物质状态不变;3.实验过程和操作方法简单易行,即选择分离提纯方法应遵循先物理后化学,先简单后复杂的原则。
本题难度:一般
4、选择题 下列装置能完成实验要求的是( )
A.
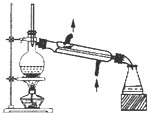
分离互不相溶的液体
B.
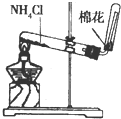
实验室制氨气
C.
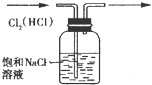
除去Cl2中的HCl
D.
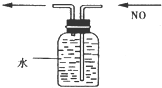
排水集气法收集NO
参考答案:C
本题解析:
本题难度:简单
5、选择题 下列有关物质分离方法的叙述中,不正确的是 [???? ]
A.用过滤的方法分离溶液和胶体
B.用蒸馏的方法将自来水制成蒸馏水
C.用四氯化碳萃取碘水中的碘
D.用加热的方法分离氯化钠和氯化铵固体
参考答案:A
本题解析:
本题难度:一般
|
|